题目内容
【题目】下面是几位同学测量空气中氧气体积分数的四个实验,请你参与他们的探究:(11分)
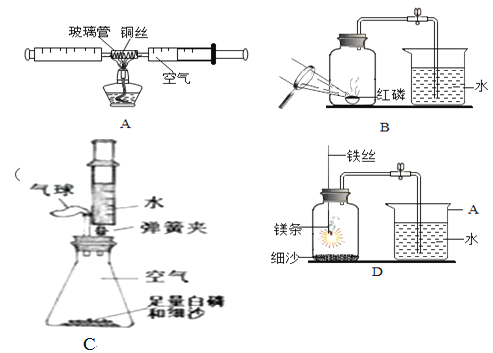
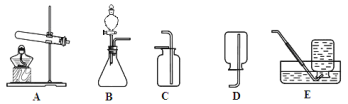
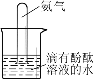
[实验一]小强采用A图所示的装置进行实验:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推拉两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是 。
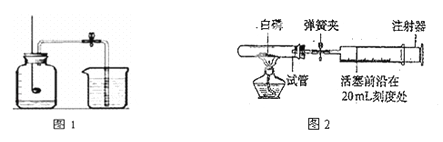
[实验二]:小红采用B图所示的装置进行实验:实验过程如下:
第一步:将集气瓶容积划分为五等份,并做好标记.
第二步:用放大镜点燃燃烧匙内的红磷.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.
请回答下列问题:
(1)集气瓶中剩余的气体主要是 ,根据实验推断它的化学性质有 。
(2)实验完毕,若进入集气瓶中水的体积小于总容积的1/5 ,其原因可能是 。
(3)红磷燃烧的现象是 ,其符号表达式为
[实验三]小华同学打算采用C图所示的装置进行实验:锥形瓶内空气体积为230mL,注射器中水的体积为50mL,该装置气密性良好。装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
请回答下列问题:
(1)在整个实验过程中,可观察到气球的变化是___________________。
(2)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:①注射器中的水自动喷射出来,②当注射器中的水还剩 mL时停止下流。
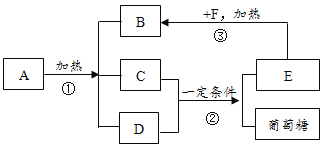
[实验四]小明用图D装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(1)冷却后打开止水夹,水能进入集气瓶的原因是 。
(2)若镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %,现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中还有 。
【答案】
实验一(1)使氧气充分反应
实验二(1)氮气,不能燃烧也不能支持燃烧;
(2)装置的气密性不好,红磷不足或没有等集气瓶冷却就打开止水夹;
(3)产生大量的白烟;P+O2![]() P2O5;
P2O5;
[实验三] (1)先鼓后瘪;(2)当注射器中的水还剩 4 mL时停止下流。
[实验四]
(1)镁条燃烧消耗氧气,不生成气体,冷却后瓶中压强减小,使水回流。
(2)21%,氮气
【解析】
试题分析:实验一(1)实验一是通过铜和氧气反应导致注射器中的压强变小,大气压强把注射器往里推断,通过注射器的读数变化来判断氧气的体积,在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使氧气充分反应,否则会导致测定的氧气的体积偏小;
实验二(1)空气主要是由氮气和氧气组成的,氧气约占空气总体积的1/5,白磷燃烧消耗氧气,故集气瓶中剩余的气体主要是氮气,氮气不能燃烧也不能支持燃烧;
(2)装置的气密性不好,红磷不足或没有等集气瓶冷却就打开止水夹均会导致测定的氧气的体积分数偏小;
(3)红磷燃烧产生大量的白烟,生成的是五氧化二磷:P+O2![]() P2O5;
P2O5;
实验三(1)白磷燃烧放出热量,消耗氧气,故能看到的现象是气球先变胀大后变瘪;
(2)氧气约占空气总体积的1/5,锥形瓶内空气体积为230mL,那么氧气的体积=230ml×1/5 =46ml,故注射器中水会有46ml进入锥形瓶中,注射器中剩余水的体积=50ml-46ml=4ml;
实验四(1)镁条燃烧消耗氧气,生成的是氧化镁,氧化镁是固体,冷却后瓶中压强减小,使水回流;
(2)氧气占空气总体积的21%,故若镁只与氧气反应,那么进入集气瓶中的水不超过21%;空气中78%的是氮气,现进入水的体积为70%,可知空气中氮气的含量一定减少了。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案