题目内容
50g质量分数为10%食盐溶液,要使其质量分数增大1倍,可采用的方法是
- A.蒸发掉一半的溶剂
- B.蒸发掉25g溶剂
- C.加入6.25g食盐
- D.加入50g 10% NaCl溶液
BD
分析:要使其10%食盐溶液质量分数增大1倍,即变成质量分数为20%的食盐溶液,使用溶质的质量分数= ,计算所提供四种方法所得溶液的溶质质量分数,质量分数为20%的方法即为可采用的方法.
,计算所提供四种方法所得溶液的溶质质量分数,质量分数为20%的方法即为可采用的方法.
解答:A、原溶液中溶剂的质量=50g-50g×10%=45g,蒸发掉一半的溶剂,即蒸发22.5g溶剂,溶质质量不变,溶液质量减小变为50g-22.5g=27.5g;此时溶液的溶质质量分数=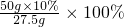 ≈18.2%≠20%;故A不正确;
≈18.2%≠20%;故A不正确;
B、蒸发掉25g溶剂,溶质质量不变,溶液质量减小为50g-25g=25g,此时溶液的溶质质量分数=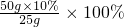 =20%;故B正确;
=20%;故B正确;
C、加入6.25g食盐,溶质质量增加,溶液质量增加,此时溶液的溶质质量分数=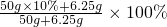 =20%;故C正确;
=20%;故C正确;
D、加入50g10%NaCl溶液,所得溶液中溶质为两溶液中溶质质量之和,溶液为两溶液质量和;
则所得溶液的溶质质量分数=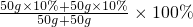 =10%≠20%;故D不正确;
=10%≠20%;故D不正确;
故选BC.
点评:溶质质量分数相等的溶液混合后所得溶液的质量分数仍为原溶液的溶质质量分数,这也是溶液具有均一性的体现.
分析:要使其10%食盐溶液质量分数增大1倍,即变成质量分数为20%的食盐溶液,使用溶质的质量分数=
 ,计算所提供四种方法所得溶液的溶质质量分数,质量分数为20%的方法即为可采用的方法.
,计算所提供四种方法所得溶液的溶质质量分数,质量分数为20%的方法即为可采用的方法.解答:A、原溶液中溶剂的质量=50g-50g×10%=45g,蒸发掉一半的溶剂,即蒸发22.5g溶剂,溶质质量不变,溶液质量减小变为50g-22.5g=27.5g;此时溶液的溶质质量分数=
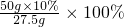 ≈18.2%≠20%;故A不正确;
≈18.2%≠20%;故A不正确;B、蒸发掉25g溶剂,溶质质量不变,溶液质量减小为50g-25g=25g,此时溶液的溶质质量分数=
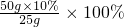 =20%;故B正确;
=20%;故B正确;C、加入6.25g食盐,溶质质量增加,溶液质量增加,此时溶液的溶质质量分数=
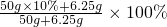 =20%;故C正确;
=20%;故C正确;D、加入50g10%NaCl溶液,所得溶液中溶质为两溶液中溶质质量之和,溶液为两溶液质量和;
则所得溶液的溶质质量分数=
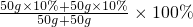 =10%≠20%;故D不正确;
=10%≠20%;故D不正确;故选BC.
点评:溶质质量分数相等的溶液混合后所得溶液的质量分数仍为原溶液的溶质质量分数,这也是溶液具有均一性的体现.

练习册系列答案
相关题目
常温下,向50g质量分数为10%的NaCl溶液中加入2g NaNO3固体并全部溶解,则溶液中NaCl的质量分数( )
| A、增大 | B、减小 | C、不变 | D、约为9.6% |
 小雪同学想制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液.请回答下列问题:
小雪同学想制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液.请回答下列问题: