题目内容
如何用化学方法除去下列物质中的杂质(括号中为杂质),写出有关的化学反应方程式.(1)Fe(Fe2O3) .
(2)Cu(Fe) .
(3)FeSO4溶液(CuSO4) .
【答案】分析:(1)根据金属氧化物可以被还原剂还原进行分析;
(2)根据金属活动性顺序进行分析;
(3)根据铁可以置换出硫酸铜中的铜进行分析.
解答:解:(1)金属氧化物可以被还原剂还原,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,故答案为:Fe2O3+3CO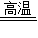 2Fe+3CO2;
2Fe+3CO2;
(2)铁位于氢之前,铜位于氢之后,铁和硫酸反应生成硫酸亚铁和氢气,故答案为:Fe+H2SO4=FeSO4+H2↑(不宜采用硫酸铜或者氯化铜,容易导致金属不纯);
(3)铁和硫酸铜反应生成硫酸亚铁和铜,故答案为:Fe+CuSO4=FeSO4+Cu.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.
(2)根据金属活动性顺序进行分析;
(3)根据铁可以置换出硫酸铜中的铜进行分析.
解答:解:(1)金属氧化物可以被还原剂还原,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,故答案为:Fe2O3+3CO
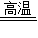 2Fe+3CO2;
2Fe+3CO2;(2)铁位于氢之前,铜位于氢之后,铁和硫酸反应生成硫酸亚铁和氢气,故答案为:Fe+H2SO4=FeSO4+H2↑(不宜采用硫酸铜或者氯化铜,容易导致金属不纯);
(3)铁和硫酸铜反应生成硫酸亚铁和铜,故答案为:Fe+CuSO4=FeSO4+Cu.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.

练习册系列答案
相关题目
如何用化学方法除去下列物质中的少量杂质,写出除杂质的试剂和发生反应的化学方程式
| 物质(杂质) | 加入试剂 | 有关化学方程式 |
| C(CuO) |