题目内容
【题目】下列图象不能正确反映其对应变化关系的是( )
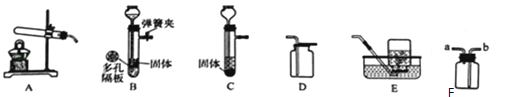
A.
某温度下将一定量接近饱和的 KNO3溶液恒温蒸发水分
B.
一定质量的红磷在密闭容器中燃烧
C.
将一瓶浓硫酸露置于空气中
D.
向一定质量的氯化镁和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
【答案】C
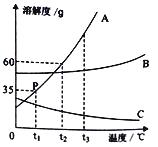
【解析】解:A、将一定质量的KNO3不饱和溶液恒温蒸发水,开始由于硝酸钾不饱和,水减少,不会析出晶体,溶质不变,所以溶质质量分数增大,对饱和溶液恒温蒸发溶剂时,由于溶剂减少,溶质也会析出,即溶液一直呈饱和状态.由于温度不变,其溶解度也不变,而饱和溶液中,溶质质量分数= ![]() ×100%,溶解度不变则溶质质量分数不变,所以溶质质量分数先增大,再不变,故正确;
×100%,溶解度不变则溶质质量分数不变,所以溶质质量分数先增大,再不变,故正确;
B、由质量守恒定律的定义可知,反应前后物质总质量不发生改变,此反应在密闭容器中进行,无其他物质的进入或散失,故物质总质量不会改变,与图象所示吻合,故B正确;
C、浓硫酸具有吸水性,敞口放置在空气中溶质质量分数减小,图象不能正确反映其对应关系,故错误;
D、盐酸和氯化镁的混合溶液呈酸性,而加入氢氧化钠不断消耗盐酸而使溶液的pH逐渐变大,至完全反应溶液pH=7;随后加入的氢氧化钠又与氯化镁反应生成氯化钠溶液和氢氧化镁沉淀,此过程中溶液的pH仍为7;直至氯化镁完全反应,继续滴入的氢氧化钠溶液过量,由于氢氧化钠溶液pH大于7,故正确;
故选:C.
【考点精析】关于本题考查的溶质的质量分数和质量守恒定律及其应用,需要了解溶质的质量分数=(溶质质量/溶液质量)*100% = [溶质质量/(溶质质量+溶剂质量]*100%;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏才能得出正确答案.

 阅读快车系列答案
阅读快车系列答案【题目】糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究.
(1)【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液在pH试纸测上并与对比,读出其pH值约为10,由此得出结论是:碳酸氢钠溶液呈碱性.
(2)【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为 . 结论:碳酸氢钠能与酸反应.
(3)【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示.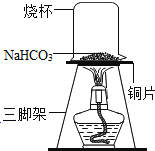
①加热一段时间后,观察到烧杯内壁有水珠.
②充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊.
③通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管.
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量 | 产生白色沉淀 | 产物含 |
② | 取操作①后的上层清液于试管B中,滴加 | 产物不含NaOH |
请分析上述操作①中不能用澄清石灰水替代氯化钙溶液的理由 .
④根据上述实验结论,写出碳酸氢钠受热分解的化学方程式 .
【题目】某品牌洁厕灵的成分是哦硫酸与盐酸的混合溶液,某课外活动小组想测定该品牌洁厕灵溶液中HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH值变化的部分数据如表所示:(已知BaCl2溶液的pH=7)
滴加氢氧化钡溶液的质量/g | 5 | 10 | 25 | 30 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 | 4.66 |
求:
(1)完全反应后生成沉淀的质量为;
(2)计算该洁厕灵溶液中HCl的质量分数为多少?(计算结果保留至0.1%)
【题目】重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地.某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示.
稀盐酸的总质量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
烧杯中物质总质量(g) | 14.66 | 24.22 | m | 43.34 | 52.90 | 62.90 | 72.90 |
(1)碳酸钙的相对分子质量为 .
(2)表中m= .
(3)求样品中碳酸钙的质量分数(结果保留两位小数).