题目内容
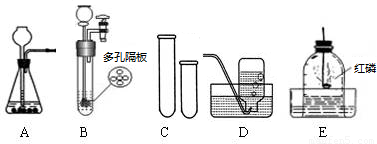
(2008?重庆模拟)某同学欲探究赤铁矿粉(主要成分Fe2O3,杂质不反应)中Fe2O3的质量分数,他利用了如下的装置:
(1)写出A中发生的化学反应方程式______ 2Fe+3CO2
【答案】分析:(1)氧化铁和一氧化碳反应能生成铁和二氧化碳;
(2)B是为了检验生成的二氧化碳是否被氢氧化钠溶液完全吸收;
(3)根据有关方面的数据可以求出氧化铁的质量分数;
(4)根据相关方面的数据可以判断具体的物质.
解答:解:(1)氧化铁和一氧化碳反应的化学方程式为:3CO+Fe2O3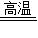 2Fe+3CO2.
2Fe+3CO2.
(2)A中反应生成的二氧化碳能够被氢氧化钠溶液吸收,B是为了检验生成的二氧化碳是否被氢氧化钠溶液完全吸收.故填:A、C、B.
如果二氧化碳进入B中,二氧化碳能和氢氧化钙反应,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(3)解设氧化铁的质量为X,
3CO+Fe2O3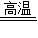 2Fe+3CO2,
2Fe+3CO2,
160 132
X wg

X=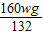
则该赤铁矿粉中Fe2O3的质量分数为: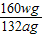 ×100%.故填:
×100%.故填: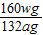 ×100%.
×100%.
(4)若测得A装置中固体质量减少了n g,则(w-n)g是参加反应的一氧化碳的质量.故填:一氧化碳.
点评:本题主要考查计算和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.
(2)B是为了检验生成的二氧化碳是否被氢氧化钠溶液完全吸收;
(3)根据有关方面的数据可以求出氧化铁的质量分数;
(4)根据相关方面的数据可以判断具体的物质.
解答:解:(1)氧化铁和一氧化碳反应的化学方程式为:3CO+Fe2O3
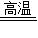 2Fe+3CO2.
2Fe+3CO2. (2)A中反应生成的二氧化碳能够被氢氧化钠溶液吸收,B是为了检验生成的二氧化碳是否被氢氧化钠溶液完全吸收.故填:A、C、B.
如果二氧化碳进入B中,二氧化碳能和氢氧化钙反应,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(3)解设氧化铁的质量为X,
3CO+Fe2O3
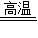 2Fe+3CO2,
2Fe+3CO2,160 132
X wg

X=
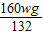
则该赤铁矿粉中Fe2O3的质量分数为:
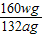 ×100%.故填:
×100%.故填: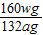 ×100%.
×100%.(4)若测得A装置中固体质量减少了n g,则(w-n)g是参加反应的一氧化碳的质量.故填:一氧化碳.
点评:本题主要考查计算和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
(2008?重庆模拟)某同学在学习了近一年的初中化学后,总结了一些说法,判断这些说法是否正确.若正确,在右边空白栏打“√”;若错误,请举出相应的例子证明.
| 说法 | 驳斥观点的事例或化学方程式 |
| 溶液都是无色的 | |
| 碱溶液中一定含有氢氧根离子 | |
| 分解反应生成物只有两种 | |
| 所有复分解反应最多只能生成一种沉淀 |