题目内容
【题目】实验室用过量的稀盐酸和大理石制取CO2 , 取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.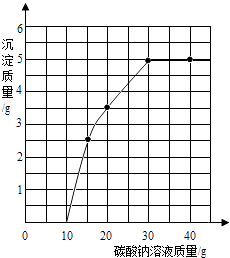
回答下列问题:
(1)从图中看出生成沉淀的最大质量是 g.
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原因是 .
(3)计算原滤液中氯化钙的质量分数.
【答案】
(1)5
(2)稀盐酸先与碳酸钠反应
(3)
解:设原滤液中CaCl2的质量为x
Na2CO3+ | CaCl2= | CaCO3↓+2NaCl |
111 | 100 | |
X | 5g |
![]()
x=5.55g
故原滤液中氯化钙的质量分数为: ![]() ×100%=11.1%
×100%=11.1%
【解析】解:(1)由图可以看出,生成沉淀的最大质量是5g;(2)因稀盐酸过量,故加入碳酸钠后首先与过量的稀盐酸反应,然后再与氯化钙反应;
【考点精析】认真审题,首先需要了解根据化学反应方程式的计算(各物质间质量比=系数×相对分子质量之比).

练习册系列答案
相关题目