题目内容
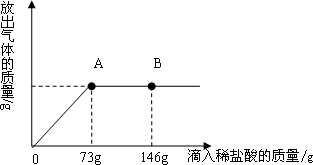
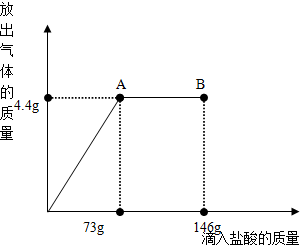 在一烧杯中盛有11.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
在一烧杯中盛有11.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH
<
<
(填>、=、<).此刻,溶液中的溶质是NaCl,HCl
NaCl,HCl
.(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数.(计算结果保留0.1%)
分析:(1)由质量关系图,当滴入稀盐酸73g时即图中A点,放出气体达最大值,溶液中碳酸钠全部反应生成氯化钠,继续滴入稀盐酸146g则酸过量,即图中B点;
(2)当滴加稀盐酸至图中A点时,烧杯中溶液恰好为中性即滴加的稀盐酸恰好与溶液中的碳酸钠完全反应,此时放出气体质量达最大值即4.4g,据此分析解答.
(2)当滴加稀盐酸至图中A点时,烧杯中溶液恰好为中性即滴加的稀盐酸恰好与溶液中的碳酸钠完全反应,此时放出气体质量达最大值即4.4g,据此分析解答.
解答:解:(1)根据质量关系图,滴入稀盐酸73g时,稀盐酸与溶液中碳酸钠全部反应生,溶液为氯化钠溶液呈中性,继续滴入稀盐酸则酸过量,中性溶液变成酸性,pH小于7,此时的溶质为氯化钠和过量的盐酸中的HCl;
(2)设固体混合物中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
=
=
x=10.6g y=11.7g
NaCl溶液中溶质的质量分数=
×100%=15.6%
故答案为:(1)<;NaCl,HCl;(2)所得溶液中溶质的质量分数是15.6%;
(2)设固体混合物中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
| 106 |
| x |
| 117 |
| y |
| 44 |
| 4.4g |
x=10.6g y=11.7g
NaCl溶液中溶质的质量分数=
| 11.7g+11.4g-10.6g |
| 11.4g+73g-4.4g |
故答案为:(1)<;NaCl,HCl;(2)所得溶液中溶质的质量分数是15.6%;
点评:本题较好的考查学生利用图象来分析化学反应的能力,学生应明确图象中的关键点及线的变化所表示的含义,将图象和化学反应紧密结合是解题的关键所在.

练习册系列答案
相关题目
在天平两端的烧杯中盛有等质量,等溶质质量分数的盐酸溶液,天平平衡.向一只烧杯中加入一定质量的镁,另一只烧杯中加入一定质量的铝,充分反应后,天平仍然平衡.则加入Mg和Al的质量比可能是( )
| A、11:12 | B、32:33 | C、33:32 | D、1:1 |
在托盘天平两盘上各放一只烧杯,两烧杯中盛有等质量分数的过量盐酸,天平两边保持平衡.此时向左边烧杯中加入11.2gCaO,若要使天平两边再次保持平衡,需向右边烧杯中加入CaCO3的质量是( )
| A、11.2g | B、17.6g | C、20g | D、22.4g |