题目内容
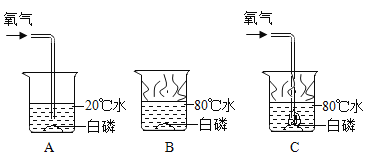
【题目】如图所示为A、B、C三种物质的溶解度曲线.
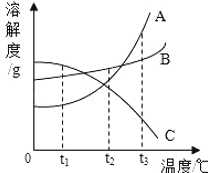
(1)t1℃时,A、B、C三种物质的溶解度大小依次为S1g、S2g、S3g.则S1、S2、S3这三个数中最大的是_____,最小的是_____;
(2)t2℃时,A的溶解度为Sg,该温度下,A的饱和溶液中,溶质的质量分数为_____;
(3)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t2℃时,所得溶液中溶质的质量分数依次为a%、b%、c%,则a、b、c由大到小的顺序是_____.
【答案】S3 S1 ![]() ×100% b>a>c
×100% b>a>c
【解析】
(1)从溶解度曲线看出,t1℃时C的溶解度最大,其次是B,A最小;
(2)在一定的温度下,某固体物质在100克溶剂里达到饱和溶液时所能溶解的质量,就是该种物质的溶解度。t2℃时,A的溶解度为Sg,就是在100g水里溶解SgA时溶液恰好达到饱和.根据溶质质量分数的概念,该溶液的溶质的质量分数为![]() ×100%;
×100%;
(3)A物质、B物质的溶解度随温度升高而增大;C物质的溶解度随温度的升高而减小.将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t2℃时,A和B溶液中有固体析出,溶质质量分数都减小,但仍是饱和溶液;C溶液变成不饱和溶液,溶质质量分数不变。又因为t2℃时B物质的溶解度比A物质的溶解度大,所以饱和溶液中溶质质量分数b>a,因为C溶液质量分数不变,而t3℃时C物质的溶解度小于t2℃时A和B物质的溶解度,可得b>a>c。

【题目】某公司生产的新型融雪剂的成分是无水CaCl2和少量的氯化钠,为测定融雪剂中氯化钙的含量,化学兴趣小组的同学称取该样品12g,加水充分溶解,得到溶液50g,然后取一定质量分数的碳酸钠溶液100g平均分五次加入,充分振荡,实验数据见表。请你分析数据并进行有关计算。
次 数 | 1 | 2 | 3 | 4 | 5 |
加入碳酸钠溶液的质量/g | 20 | 20 | 20 | 20 | 20 |
生成沉淀的质量/g | 2.5 | x | 7.5 | 10 | 10 |
(1)上表中x的数值为_____。第_____次加入的碳酸钠与氯化钙恰好完全反应。
(2)样品中氯化钙的质量分数是多少_____?
(3)恰好完全反应时过滤,所得不饱和溶液的溶质质量分数是多少_____?