题目内容
某金属氧化物R2O能与水反应生成ROH.已知在R2O中R元素与氧元素的质量比为23:8,现将质量为m的水加到6.2g该金属氧化物中,得到溶质的质量分数为16%的溶液.试求:(1)该金属元素R的相对原子质量;
(2)加到该金属氧化物中水的质量m.
【答案】分析:(1)可以根据元素质量比和氧元素的相对原子质量解出R的相对原子质量;
(2)根据题中的数据找出比例关系进行解答.
解答:解:(1)设R的相对原子质量为X,
(2X):16=23:8
X=23,
(2)设6.2克的金属氧化物消耗水为y,生成氢氧化钠为z,
Na2O+H2O=2NaOH
62 18 80
6.2g Y Z
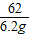 =
=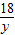 =
=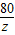
y=1.8g
z=8g
所以氢氧化钠溶液质量为: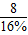 =50g,
=50g,
所以水的质量为:50g-8g+1.8g=43.8克,
答:R的相对原子质量为23,水的质量m为43.8克.
点评:在解此类题时,首先分析题中考查的问题,然后结合题中所给的数据列出比例关系求出相关的数据进行解答.
(2)根据题中的数据找出比例关系进行解答.
解答:解:(1)设R的相对原子质量为X,
(2X):16=23:8
X=23,
(2)设6.2克的金属氧化物消耗水为y,生成氢氧化钠为z,
Na2O+H2O=2NaOH
62 18 80
6.2g Y Z
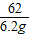 =
=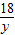 =
=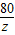
y=1.8g
z=8g
所以氢氧化钠溶液质量为:
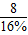 =50g,
=50g,所以水的质量为:50g-8g+1.8g=43.8克,
答:R的相对原子质量为23,水的质量m为43.8克.
点评:在解此类题时,首先分析题中考查的问题,然后结合题中所给的数据列出比例关系求出相关的数据进行解答.

练习册系列答案
相关题目