题目内容
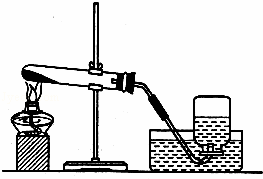
使用如图所示装置制取氧气。
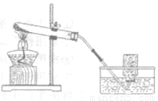
(1)写出加热高锰酸钾制氧气的化学方程式: ;
(2)指出图4装置中1个明显的不足之处: ;
(3)氧气收集完成后,测得其纯度明显偏低,原因可能是: (填字母,可多选);
A.高锰酸钾中混入了二氧化锰
B.收集前,集气瓶中未注满水
C.收集后,集气瓶中仍有少量水
D.未见气泡连续均匀冒出时应开始收集
(4)在研究“适于制取氧气的物质及其反应条件”的过程中,某同学完成了如表所示的系列实验:
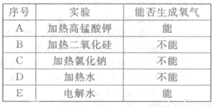
①根据实验A、B、C,可以得出的结论是:在一定条件下, ;
②根据实验D、E,可以得出的结论是: 是影响物质能否反应产生氧气的重要因素;
(5)将10g高锰酸钾加热一段时间后,称得剩余固体的质量为9.36g。试计算:
①产生氧气的质量;
②剩余高锰酸钾的质量。
(1)2KMnO4高温 K2MnO4+MnO2+O2↑; (2)试管口没放一团棉花; (3)BD;
(4)①像高锰酸钾这样能反应产生氧气的物质才适于制氧气; ②反应条件;
(5)①产生氧气的质量为10g-9.36g=0.64g; ②3.68g。
【解析】
试题分析:(1)加热高锰酸钾制氧气的化学方程式:2KMnO4高温K2MnO4+MnO2+O2↑;
(2)加热高锰酸钾制氧气时应在试管口放一团棉花,防止固体粉末堵塞导管。图4装置没有。
(3)氧气收集完成后,测得其纯度明显偏低。说明收集的氧气中混有空气。其可能的原因为B(集气瓶中原有部分空气)D(开始收集的气体是装置内的空气)。
(4)①对比ABC可知,只有A产生了氧气,BC均没有生成氧气。所以可得出“在一定条件下,像高锰酸钾这样能反应产生氧气的物质才适于制氧气”;
②对比实验D、E:二者反应物都是水。但在不同的条件下D没有生成氧气;E生成了氧气。所以可以得出的结论是:反应条件是影响物质能否反应产生氧气的重要因素;
(5)①根据质量守恒定律可知:产生氧气的质量为10g-9.36g=0.64g;
②分析:已知生成氧气的质量,未知剩余高锰酸钾的质量。可先根据氧气的质量求出参与反应的高锰酸钾的质量。具体解题过程为:
设参与反应的高锰酸钾的质量为x
2KMnO4高温 K2MnO4+MnO2+O2↑
316 32
x 0.64g
316:32=x:0.64g
x=6.32g
剩余高锰酸钾的质量为:10g-6.32g=3.68g。
考点:气体的制备
点评:能够正确地应用气体制备知识进行解答。

 名校课堂系列答案
名校课堂系列答案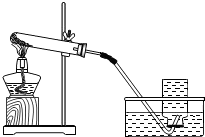 使用如图所示装置制取氧气.
使用如图所示装置制取氧气.
(1)写出加热高锰酸钾制氧气的化学方程式:______:
(2)指出右图装置中一个明显的不足之处:______;
(3)氧气收集完成后,测得其纯度明显偏低,原因可能是:______(填字母、可多选);
A.高锰酸钾中混入了二氧化锰
B.收集前,集气瓶中未注满水
C.收集后,集气瓶中仍有少量水
D.未见气泡连续均匀冒出时就开始收集
(4)在研究“适于制取氧气的物质及其反应条件”的过程中,某同学完成了下表所示系列实验:
| 序号 | 实验 | 能否生成氧气 |
| A | 加热高锰酸钾 | 能 |
| B | 加热二氧化硅 | 不能 |
| C | 加热氯化钠 | 不能 |
| D | 加热水 | 不能 |
| E | 电解水 | 能 |
②根据实验D、E,可以得出的结论是:______是影响物质能否反应产生氧气的重要因素;
(5)将10g高锰酸钾加热一段时间后,称得剩余固体的质量为9.36g.试计算:
①产生氧气的质量;
②剩余高锰酸钾的质量.
使用如图所示装置制取氧气.
(1)写出加热高锰酸钾制氧气的化学方程式: :
(2)指出右图装置中一个明显的不足之处: ;
(3)氧气收集完成后,测得其纯度明显偏低,原因可能是: (填字母、可多选);
A.高锰酸钾中混入了二氧化锰
B.收集前,集气瓶中未注满水
C.收集后,集气瓶中仍有少量水
D.未见气泡连续均匀冒出时就开始收集
(4)在研究“适于制取氧气的物质及其反应条件”的过程中,某同学完成了下表所示系列实验:
| 序号 | 实验 | 能否生成氧气 |
| A | 加热高锰酸钾 | 能 |
| B | 加热二氧化硅 | 不能 |
| C | 加热氯化钠 | 不能 |
| D | 加热水 | 不能 |
| E | 电解水 | 能 |
①根据实验A、B、C,可以得出的结论是:在一定条件下, ;
②根据实验D、E,可以得出的结论是: 是影响物质能否反应产生氧气的重要因素;
(5)将10g高锰酸钾加热一段时间后,称得剩余固体的质量为9.36g.试计算:
①产生氧气的质量;
②剩余高锰酸钾的质量.
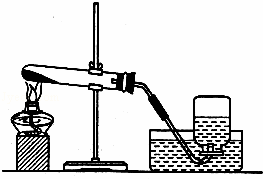
使用如图所示装置制取氧气.
(1)写出加热高锰酸钾制氧气的化学方程式: :
(2)指出右图装置中一个明显的不足之处: ;
(3)氧气收集完成后,测得其纯度明显偏低,原因可能是: (填字母、可多选);
A.高锰酸钾中混入了二氧化锰
B.收集前,集气瓶中未注满水
C.收集后,集气瓶中仍有少量水
D.未见气泡连续均匀冒出时就开始收集
(4)在研究“适于制取氧气的物质及其反应条件”的过程中,某同学完成了下表所示系列实验:
| 序号 | 实验 | 能否生成氧气 |
| A | 加热高锰酸钾 | 能 |
| B | 加热二氧化硅 | 不能 |
| C | 加热氯化钠 | 不能 |
| D | 加热水 | 不能 |
| E | 电解水 | 能 |
①根据实验A、B、C,可以得出的结论是:在一定条件下, ;
②根据实验D、E,可以得出的结论是: 是影响物质能否反应产生氧气的重要因素;
(5)将10g高锰酸钾加热一段时间后,称得剩余固体的质量为9.36g.试计算:
①产生氧气的质量;
②剩余高锰酸钾的质量.
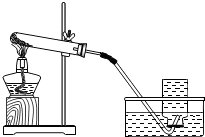 (2013?常州)使用如图所示装置制取氧气.
(2013?常州)使用如图所示装置制取氧气.