题目内容
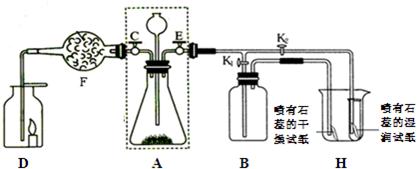
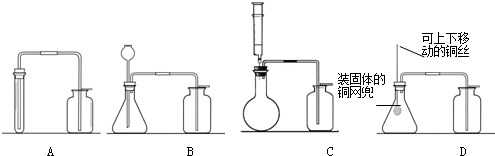
下列为二氧化碳制取和性质实验的组合装置图,已知A中为盐酸和石灰石,请根据如图所示回答相关问题.(假设各步均充分反应)
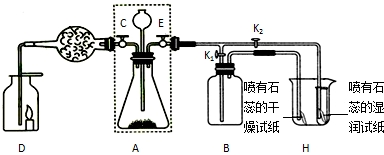
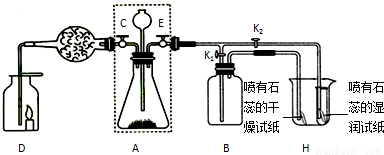
请根据上述实验如图所示,写出该实验的目的是______.
若关闭K2打开K1,装置B中盛放的药品是______;若关闭K1打开K2,可看到的实验现象是______.
(2)关闭E、打开C时,若F中盛放的是干燥剂,观察到D中的蜡烛熄灭,说明二氧化碳具有______的性质.
(3)关闭E打开C时,若F中盛放的是过氧化钠(Na2O2),则观察到D中的蜡烛燃烧得更旺,说明有氧气生成.
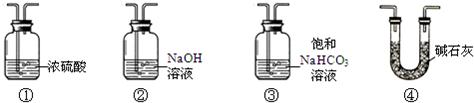
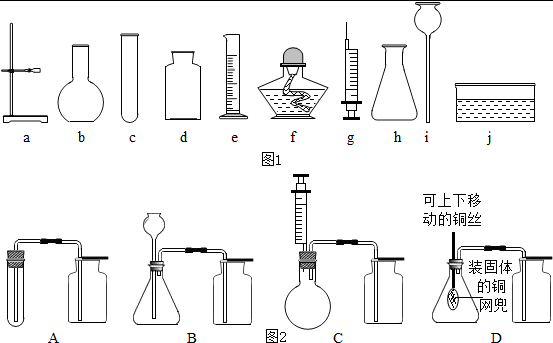
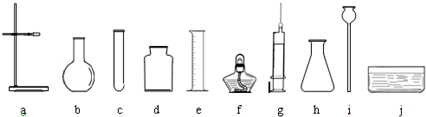
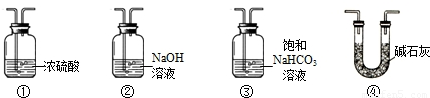
小明查阅资料得知:过氧化钠与二氧化碳、氯化氢气体、水等均能发生反应生成氧气.为确认二氧化碳与过氧化钠反应产生氧气,他对装置进行了改进,有如下备选装置:
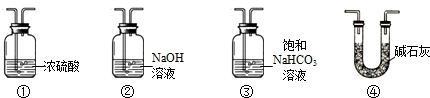
他的连接顺序为:A→______→F.小明还证明了反应后F中含有碳酸钠,写出二氧化碳与过氧化钠(Na2O2)反应的化学方程式______.
解:(1)①该实验的目的是证明二氧化碳是否与水反应;②设计实验:让二氧化碳分别到达干燥和湿润的试纸上,看是否变色;从而判断二氧化碳是否与水反应生成碳酸;
(2)观察到D中的蜡烛熄灭,说明二氧化碳具有不能燃烧也不支持燃烧的性质;
(3)通过碳酸氢钠溶液,除掉氯化氢气体;通过浓硫酸吸收掉水分;这就排除了氯化氢气体和水的干扰,F中含有碳酸钠,所以A→③①→F,只有过氧化钠与二氧化碳反应了.
故答为:(1)证明二氧化碳是否与水反应;浓硫酸;湿润的石蕊试纸变红色
(2)不能燃烧也不支持燃烧
(3)A→③①→F;2CO2+2Na2O2═2Na2CO3+O2
分析:(1)已知A中为盐酸和石灰石,上图二氧化碳制取和性质实验的组合装置图,①该实验的目的是证明二氧化碳是否与水反应;
②若关闭K2打开K1,装置B中盛放的药品是干燥剂,为浓硫酸;二氧化碳不能使干试纸变色,说明无碳酸生成;③若关闭K1打开K2,二氧化碳到达湿润的试纸上,可看到的实验现象是湿润的石蕊试纸变红色,说明有碳酸生成;
(2)观察到D中的蜡烛熄灭,说明二氧化碳具有不能燃烧也不支持燃烧的性质;
(3)①用碳酸钙和盐酸反应制取二氧化碳,气体中会混有氯化氢气体,所以通过碳酸氢钠溶液,除掉氯化氢气体;②通过浓硫酸吸收掉水分,排除水的干扰,因为“过氧化钠与二氧化碳、氯化氢气体、水等均能发生反应生成氧气”所以A→③①→F(F中含有碳酸钠),这样过氧化钠只与二氧化碳反应,所以可写出化学方程式.
点评:本题主要考查了二氧化碳的实验室制法(装置及原理),掌握二氧化碳的化学性质及其应用.
(2)观察到D中的蜡烛熄灭,说明二氧化碳具有不能燃烧也不支持燃烧的性质;
(3)通过碳酸氢钠溶液,除掉氯化氢气体;通过浓硫酸吸收掉水分;这就排除了氯化氢气体和水的干扰,F中含有碳酸钠,所以A→③①→F,只有过氧化钠与二氧化碳反应了.
故答为:(1)证明二氧化碳是否与水反应;浓硫酸;湿润的石蕊试纸变红色
(2)不能燃烧也不支持燃烧
(3)A→③①→F;2CO2+2Na2O2═2Na2CO3+O2
分析:(1)已知A中为盐酸和石灰石,上图二氧化碳制取和性质实验的组合装置图,①该实验的目的是证明二氧化碳是否与水反应;
②若关闭K2打开K1,装置B中盛放的药品是干燥剂,为浓硫酸;二氧化碳不能使干试纸变色,说明无碳酸生成;③若关闭K1打开K2,二氧化碳到达湿润的试纸上,可看到的实验现象是湿润的石蕊试纸变红色,说明有碳酸生成;
(2)观察到D中的蜡烛熄灭,说明二氧化碳具有不能燃烧也不支持燃烧的性质;
(3)①用碳酸钙和盐酸反应制取二氧化碳,气体中会混有氯化氢气体,所以通过碳酸氢钠溶液,除掉氯化氢气体;②通过浓硫酸吸收掉水分,排除水的干扰,因为“过氧化钠与二氧化碳、氯化氢气体、水等均能发生反应生成氧气”所以A→③①→F(F中含有碳酸钠),这样过氧化钠只与二氧化碳反应,所以可写出化学方程式.
点评:本题主要考查了二氧化碳的实验室制法(装置及原理),掌握二氧化碳的化学性质及其应用.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目