题目内容
16.某兴趣小组用氯酸钾和二氧化锰的化合物加热制取氧气,试管中固体的质量随时间变化的数据见下表.| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(2)剩余物质各是什么?质量分别为多少克?
分析 氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算氯酸钾的质量和生成的氯化钾的质量,即可解答.
解答 解:(1)由表中的数据可知,共制得氧气的质量为:28.0g-18.4g=9.6g,故填9.6;
(2)设反应生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 9.6g
$\frac{149}{x}=\frac{96}{9.6g}$
x=14.9g
二氧化锰质量为:18.4g-14.9g=3.5g
答:剩余物质中氯化钾的质量14.9g;二氧化锰的质量是3.5g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,难度不大,计算时要注意规范性和准确性.

练习册系列答案
相关题目
6.燃着的火柴梗火焰一端向上竖直放置,火柴梗不易继续燃烧,其原因是火柴未燃烧部分( )
| A. | 温度达不到着火点 | B. | 着火点高 | ||
| C. | 着火点低 | D. | 接触氧气少 |
11.下列实验现象的描述正确的是( )
| A. | 向装有大理石的试管中加入适量稀盐酸产生二氧化碳 | |
| B. | 铁丝在空气中剧烈燃烧、火星四射,生成黑色固体物质 | |
| C. | 硫在氧气中燃烧发出明亮蓝紫色火焰 | |
| D. | 雪碧摇一摇再打开瓶盖,会看到二氧化碳气体喷出 |
1.下列有关催化剂的说法正确的是( )
| A. | MnO2是催化剂,为加快反应速率,在化学反应里都应用它做催化剂 | |
| B. | 要使KClO3受热分解放出氧气,必须加入MnO2,否则就不能产生O2 | |
| C. | 向H2O2溶液中加入MnO2可以使产生的氧气量增多 | |
| D. | 不同的化学反应可选用不同的催化剂,催化剂可以加快反应速率,也可以减缓反应速率 |
8.同学们在学习了木炭还原氧化铜的实验后,联想到单质碳的一些化学性质,对反应后的气体成分产生了疑问,某学习小组对该反应产物中的气体成分进行了探究.
〔猜 想〕
①气体产物全部是CO2 ②气体产物全部是CO ③气体产物气体产物是CO和CO2的混合物
〔查阅资料〕CO气体能使湿润的黄色氯化钯试纸变蓝色.
〔设计实验〕根据各自的猜想,他们共同设计了如图的实验装置进行探究.

〔现象与分析〕
〔结论〕实验现象证明猜想③成立,同学们的疑问是合理的.
〔反思〕
(1)同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②原因二:反应中的一种产物和反应物木炭又发生了化学反应,产生了CO;
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO或CuO+C$\frac{\underline{\;高温\;}}{\;}$Cu+CO.
(2)根据上述实验,请你归纳出单质碳在工业上的重要用途单质碳在工业上的重要用是途冶炼金属
(3)从环保角度考虑,该套实验装置的明显缺陷是没有尾气处理.
〔猜 想〕
①气体产物全部是CO2 ②气体产物全部是CO ③气体产物气体产物是CO和CO2的混合物
〔查阅资料〕CO气体能使湿润的黄色氯化钯试纸变蓝色.
〔设计实验〕根据各自的猜想,他们共同设计了如图的实验装置进行探究.

〔现象与分析〕
| 现象 | 结论 |
| 如果装置B如果装置B澄清石灰水变浑浊,装置C无现象,装置C无现象 | 则猜想①成立 |
| 如果如果装置B无现象,装置C试纸由黄色变为蓝色 | 则猜想②成立 |
| 如果如果装置B澄清石灰水变浑浊,装置C试纸由黄色变为蓝色 | 则猜想③成立 |
〔反思〕
(1)同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②原因二:反应中的一种产物和反应物木炭又发生了化学反应,产生了CO;
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO或CuO+C$\frac{\underline{\;高温\;}}{\;}$Cu+CO.
(2)根据上述实验,请你归纳出单质碳在工业上的重要用途单质碳在工业上的重要用是途冶炼金属
(3)从环保角度考虑,该套实验装置的明显缺陷是没有尾气处理.
5.下列情况一定会发生化学变化的是( )
| A. | 产生气体 | |
| B. | 两种物质混合 | |
| C. | 分子被破坏,原子重新组合成新的分子 | |
| D. | 一种物质的分子进入到另一种物质的分子中间 |
6.在学习“石灰石和钟乳石”时,小明和老师做了如图1所示的一组对比实验.
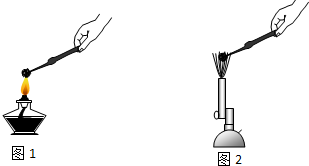
根据上述实验回答下列问题:
(1)小明的实验现象说明石灰石灼烧时没有反生化学反应,其本质原因是加热的温度不够,碳酸钙没有分解;
(2)老师的实验中酚酞溶液变红,说明溶液呈碱性,用化学方程式表示其原因CaO+H2O=Ca(OH)2
(3)若老师实验时夹持的石灰石质量为10克,灼烧完全后剩余固体为5.6克(所含杂质在灼烧过程中不发生变化),请回答下列问题:
①当石灰石完全反应后,生成CO2的物质的量为0.1mol;
②求该石灰石中CaCO3的物质的量(根据化学方程式列式计算)0.1mol.

| 实验操作 | 实验现象 | |
| 小明 | 用坩埚钳夹持一小块石灰石,在酒精灯的火焰上灼烧(如图1所示),2分钟后,把它投入含有酚酞的蒸馏水中 | 酚酞溶液不变色 |
| 老师 | 用坩埚钳夹持一小块石灰石,在酒精喷灯火焰上灼烧(如图2所示),2分钟后,把它投入含有酚酞的蒸馏水中 | 酚酞溶液变红 |
(1)小明的实验现象说明石灰石灼烧时没有反生化学反应,其本质原因是加热的温度不够,碳酸钙没有分解;
(2)老师的实验中酚酞溶液变红,说明溶液呈碱性,用化学方程式表示其原因CaO+H2O=Ca(OH)2
(3)若老师实验时夹持的石灰石质量为10克,灼烧完全后剩余固体为5.6克(所含杂质在灼烧过程中不发生变化),请回答下列问题:
①当石灰石完全反应后,生成CO2的物质的量为0.1mol;
②求该石灰石中CaCO3的物质的量(根据化学方程式列式计算)0.1mol.
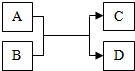 A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).(1)若A为一氧化碳,C为金属,则D为CO2;
A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).(1)若A为一氧化碳,C为金属,则D为CO2;