题目内容
【题目】下图表示某些物质间转化关系。G为常见金属,E为红棕色固体;C、F都是由相同元素组成的无色气体,且C有毒;D、H都是无色气体单质;反应⑤是自然界中最重要的反应。

请回答下列问题:
(1)B的化学式为____________。
(2)生活中为防止反应④的发生,可采取的措施是______________(写一点即可)。
(3)自然界中普遍存在反应⑤,其名称为____________________。
(4)反应①的化学方程式为________________________________,反应③的化学方程式为_______________________________。
(5)若只用C和D两气体,按一定分子数之比通过化合反应得到相应产物,则不可能得到的物质是____________(填字母序号)。
A.CH2O B.C2H6O C.CH4O
【答案】 H2O 保持铁制品表面清洁干燥 光合作用 CH4+H2O ![]() CO+3H2 2H2O
CO+3H2 2H2O![]() 2H2↑+O2↑ B
2H2↑+O2↑ B
【解析】根据所学知识和题中信息知,B是水,通电分解为氢气和氧气;G为常见金属铁,E为红棕色固体氧化铁;C、F都是由相同元素组成的无色气体,且C有毒,C是一氧化碳,F是二氧化碳;D、H都是无色气体单质,D是氢气;反应⑤是自然界中最重要的反应,H是氧气,I是碳。(1)B的化学式为H2O。(2)生活中为防止反应④铁生锈的发生,可采取的措施是保持铁制品表面清洁干燥。(3)自然界中普遍存在反应⑤,其名称为光合作用。(4)反应①的化学方程式为CH4+H2O ![]() CO+3H2,反应③的化学方程式为2H2O
CO+3H2,反应③的化学方程式为2H2O![]() 2H2↑+O2↑。(5)若只用C和D两气体,按一定分子数之比通过化合反应得到相应产物,则不可能得到的物质是C2H6O,根据质量守恒定律,若生成C2H6O,则该反应无法配平。
2H2↑+O2↑。(5)若只用C和D两气体,按一定分子数之比通过化合反应得到相应产物,则不可能得到的物质是C2H6O,根据质量守恒定律,若生成C2H6O,则该反应无法配平。
点睛∶掌握常见物质的性质是对学生的基本要求,是做好本题的重要前提。

【题目】常温下,小明同学在练习“金属的化学性质”实验操作时,发现几支试管中冒出气泡的速率有快有慢,于是他与小芳同学一起合作进行如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【猜想与假设】A.可能与酸的浓度有关;B.可能与金属的种类有关;C.可能与金属的形状有关。
【设计并实验】小明和小芳进行如下实验。
实验 编号 | 盐酸的 浓度 | 金属 (均取2 g) | 金属的 形状 | 收集50 mL 氢气所需要 的时间/s |
① | 10% | 镁 | 粉状 | 60 |
② | 10% | 铁 | 片状 | 120 |
③ | 10% | 镁 | 片状 | 102 |
④ | 20% | 铁 | 片状 | 110 |
(1)实验时需将镁片和铁片进行打磨,其目的是____________________________。
(2)写出铁与稀盐酸反应的化学方程式:________________________________。
【收集证据】
(3)要比较金属的种类对反应快慢的影响,应选择的实验编号是________。
【得出结论】通过上述四个实验,你得出的影响金属与酸反应的因素有____________________。
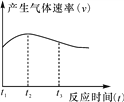
(4)实验①中试管外壁发烫,说明镁与稀盐酸反应是放热反应。实验测得镁与稀盐酸反应中产生气体的速率(v)与时间(t)的关系如图所示,你认为在t1~t2 时间段内反应速率逐渐加快的主要原因是_________________, t2~t3时间段内反应速率逐渐减慢的主要原因是___________________。