题目内容
【题目】某同学为测量某大理石产品中 CaCO3 含量,称取了 10g 该大理石样品,再加入足量的 盐酸,发现反应后质量一共减少了 3.3g(设其它杂质与盐酸不反应,不考虑 CO2 在水中 溶解),请你帮他计算:
(1)生成的 CO2 质量是_____g.
(2)该样品中 CaCO3 的质量分数_____。
【答案】3.3 75%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钙和HCl的质量,进而求算对应的质量分数。
解:(1)根据质量守恒定律,二氧化碳的质量为 3.3g;
(2)设该石灰石样品中碳酸钙的质量分数为x,
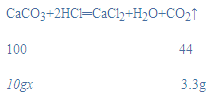
![]()
x=75%;
答:(1)生成的CO质量是 3.3g;(2)该样品中 CaCO3 的质量分数为 75%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
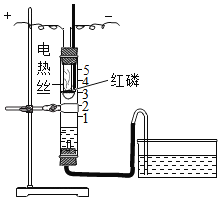
【题目】利用如图装置进行空气中氧气含量测定实验。
实验装置 | 实验操作 |
| I.向玻璃管和水槽内加适量的水,在燃烧匙里放足量红磷,塞紧塞子,上下移动水槽至两边水面相平于玻璃管的零刻度位置。 II.接通电源,待红磷燃烧,断开电源。 III.当温度恢复至室温,水不再进入玻璃管时,上下移动水槽至两边水面相平。 |
(1)实验中加入足量红磷的目的是_____,该实验中发生反应的化学方程式为_____。
(2)实验结束后,玻璃管内水面最终到达刻度线_____(填数字序号)处。
(3)实验操作I、III中,上下移动水槽至两边水面相平的目的是_____。