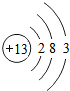题目内容
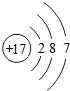
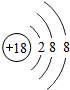
19、已知元素周期表中第三周期各元素原子结构示意图如下,请回答:

(1)在化学反应中,钠元素的原子容易失去电子变成
(2)元素的化学性质与原子结构中的
(3)从原子结构方面看:同一周期的元素具有相同的
(4)在此周期中,各元素的原子结构呈现的变化规律是:
(5)氯离子(Cl-)的结构示意图为: .
.

(1)在化学反应中,钠元素的原子容易失去电子变成
阳
(填“阴”或“阳”)离子;(2)元素的化学性质与原子结构中的
最外层电子
数关系密切;(3)从原子结构方面看:同一周期的元素具有相同的
电子层
数;(4)在此周期中,各元素的原子结构呈现的变化规律是:
原子的质子数(或最外层电子数)
依次递增.(5)氯离子(Cl-)的结构示意图为:

分析:(1)原子得到电子后,核外电子数大于质子数,微粒带负电称为阴离子;失电子后,核外电子数小于质子数,微粒带正电,称为阳离子;
(2)元素的化学性质:最外层电子数为8的微粒,化学性质稳定称为稳定结构,最外层电子小于4易失电子,大于4易得电子;
(3)比较图中同一周期内原子结构示意图,找出同一周期的元素原子结构示意图中的相同处;
(4)比较同周期中原子结构示意图,找出依次递增的数值;
(5)氯离子(Cl-)带一个单位负电荷,即得到一个电子形成的.
(2)元素的化学性质:最外层电子数为8的微粒,化学性质稳定称为稳定结构,最外层电子小于4易失电子,大于4易得电子;
(3)比较图中同一周期内原子结构示意图,找出同一周期的元素原子结构示意图中的相同处;
(4)比较同周期中原子结构示意图,找出依次递增的数值;
(5)氯离子(Cl-)带一个单位负电荷,即得到一个电子形成的.
解答:解:(1)钠元素的原子容易失去最外层的一个电子,质子数不变仍为11,电子数变成2+8=10,质子数比电子数多1,粒子带正电,为阳离子;
故答:阳;
(2)元素的化学性质取决于原子结构中的最外层电子数;
故答:最外层电子;
(3)图中所列第三周期各元素原子核外电子都分为三层,同一周期的元素具有相同的电子层数;
故答:电子层;
(4)在此周期中,各元素的原子质子数从11到18逐渐增加、最外层电子数从1到8逐渐增加;
故答:原子的质子数(或最外层电子数);
(5)氯原子得1个电子后形成氯离子(Cl-),即最外层电子数由7个变成8个,其它不变;
故答: .
.
故答:阳;
(2)元素的化学性质取决于原子结构中的最外层电子数;
故答:最外层电子;
(3)图中所列第三周期各元素原子核外电子都分为三层,同一周期的元素具有相同的电子层数;
故答:电子层;
(4)在此周期中,各元素的原子质子数从11到18逐渐增加、最外层电子数从1到8逐渐增加;
故答:原子的质子数(或最外层电子数);
(5)氯原子得1个电子后形成氯离子(Cl-),即最外层电子数由7个变成8个,其它不变;
故答:
 .
.点评:原子得电子变成阴离子,质子数不变,电子层数不变;失去最外层电子变成阳离子,质子数不变,电子层数减少.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


 16、元素周期表是学习和研究化学的重要工具.请完成下列问题:
16、元素周期表是学习和研究化学的重要工具.请完成下列问题: