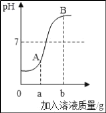
题目内容
【题目】化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图所示(假设铁片除有Fe2O3外,不含其他杂质)。
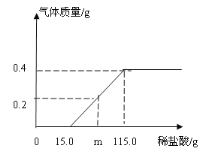
(1)m的值为________;
(2)该铁片中Fe2O3的质量分数___(写出计算过程)。
【答案】65.0 12.5%
【解析】
(1)根据图可以看出生成的氢气的质量为0.4g,生成氢气对应的盐酸溶液的质量为115.0g-15.0g=100.0g,则生成0.2g的氢气需要盐酸50.0g,因此m的值为:15.0g+50.0g=65.0g;故填:65.0
(2)设该铁片中Fe2O3的质量分数为x。
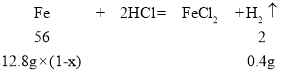
![]()
x=12.5%
答:该铁片中Fe2O3的质量分数为12.5%。故填:12.5%

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】过氧化钙(CaO2)是一种环境友好型供氧剂,可用于鱼类养殖、农作物栽培等,实验室有一瓶放置一段时间的过氧化钙样品,某兴趣小组对其成分展开了如下探究。
[查阅资料)CaO2能与水反应最终生成Ca(OH)2和O2也能与CO2反应得到 CaCO3和O2.过氧化氢溶液具有漂白性。
[提出问题]该固体样品的成分是什么?
[猜想假设]可能是CaO2、Ca(OH)2、CaCO3中的一种或几种。
[实验探究]
实验编号 | 实验步骤 | 实验现象 |
① | 取少量样品于试管中,加入一定量的水,一段时间后,在试管口插入带火星的木条 | 得到浊液,有气泡产生,木条复燃 |
② | 另取少量样品于试管中,滴加适量的试剂X,并将产生的气体通入澄清石灰水 | 得到澄清溶液有气泡产生,生成的气体使石灰水变浑浊 |
③ | 室温下,取①中上层清液,用试纸测定 溶液的pH | pH约为12 |
[得出结论]
(1)由实验1、2可知,白色固体中肯定有_____;
(2)实验2中所加试剂X可以是_____(填字母序号)。
A 稀硫酸
B 稀盐酸
C 稀硝酸
D 水
(3)根据实验3_____(填“能”或者“不能”)判断原固体样品中含有Ca(OH)2理由是_____。
[反思交流]
(4)过氧化钙敞口放置在空气中,最终会变质为_____(填化学式),原因是_____。
(5)该兴趣小组在老师指导下,用装置甲进行少量过氧化钙样品与足量水反应的实验,实验时加入过氧化钙样品与足量水,迅速密闭装置,开始测氧气浓度。滴入几滴酚酞试液,观察到三颈烧瓶中溶液先变红后慢慢褪色。620秒时,将气球内二氧化锰加入三颈烧瓶中,瓶内氧气浓度随反应时间变化如图乙。
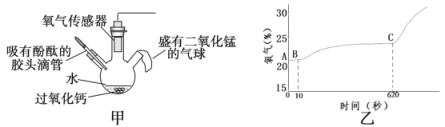
①AB段氧气浓度几乎不变的原因可能是_____;
②滴入酚酞试液后,三颈烧瓶中溶液变红后会慢慢褪色的原因可能是_____;
③写出BC段可能发生反应的化学方程式_____。
【题目】请完成下列实验,回答问题。
(1)某同学将氢气与空气混合,在安全保障下在老师指导下点燃,实验如下
V(H2)/V(空气) | 1:99 | 3:97 | 4:96 | 50:50 | 70:30 | 75:25 |
点火 | 不炸 | 不炸 | 炸 | 炸 | 炸 | 不炸 |
①该实验说明氢气的爆炸极限范围可能为______~______之间(用百分数表示)
②鉴于该实验爆炸的危险性,说明点燃氢气前必须验纯,验纯的操作为_____
③该实验证明水是由__________________组成的。
(2)除去下列物质中的杂质,所用试剂错误的是___
选项 | 物质 | 杂质 | 除杂试剂 |
A | 铜 | 氧化铜 | 稀硫酸 |
B | 二氧化碳 | 水蒸气 | 生石灰 |
C | 盐酸 | 硫酸 | 氯化钡溶液 |
D | 氯化钡溶 | 氯化钠溶液 | 碳酸钠溶液 |
【题目】在学习盐酸的化学性质时,甲、乙两位同学分别做了稀盐酸和碳酸钠溶液反应的实验(如图1)。
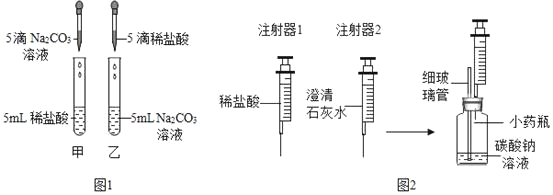
(实验现象)甲同学的实验中溶液有气泡冒出,乙同学的实验中溶液无气泡冒出。
(1)写出甲同学实验的化学反应方程式:_____。
(提出问题)乙同学的实验中溶液为什么没有气泡冒出?
(查阅资料)碳酸钠和稀盐酸反应不仅可以生成二氧化碳还可以生成碳酸氢钠
(实验)同学们设计并进行了如图2所示的实验(装置气密性良好)。
实验编号 | 实验步骤 | 实验现象 |
① | Ⅰ.用注射器1向小药瓶中缓慢注入少量的稀盐酸,边注入边振荡 | 细玻璃管中液柱略微升高 |
Ⅱ.换注射器2从瓶中缓慢抽取气体 | 澄清石灰水无明显变化 | |
② | Ⅰ.用注射器1向小药瓶中继续注入稀盐酸至较多气泡产生 | 细玻璃管中液柱明显升高 |
Ⅱ.换注射器2从瓶中缓慢抽取气体 | 澄清石灰水变浑浊 |
(2)细玻璃管在实验中的主要作用是_____;实验①中细玻璃管中液柱略微升高的原因:少量稀盐酸滴入导致小药瓶内气体体积略微压缩,_____。
(3)实验②中Ⅰ的现象是_____;实验①、②中步骤Ⅱ:注射器2必须缓慢地从瓶中抽取气体的原因是_____。
(实验反思)此反应说明反应物的量不同,产物可能不同,试另举一例:_____。
(若正确回答下列问题加4分,总分不超过60分)
在老师的帮助下,同学们利用pH传感器对相同浓度的碳酸钠溶液(pH为12)、碳酸氢钠溶液(pH为8.2)与稀盐酸反应时,pH的变化与盐酸体积的关系进行了测定,并做了如图3所示的对比图:
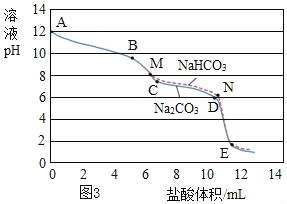
图中各线段实验现象如下表:
溶液 | 线段 | 实验现象 |
Na2CO3 | AB | 无气泡 |
BC | 有少量气泡 | |
CD | 有大量气泡 | |
DE | 几乎无气泡 | |
NaHCO3 | MN | 立即有大量气泡 |
NE | 几乎无气泡 |
(4)在AB段,溶液中的溶质有_____、_____、_____。
(5)分析图表,体现碳酸钠与稀盐酸反应分两步:
第一步反应:Na2CO3 +HCl=NaCl+NaHCO3
第二步反应的化学方程式为:_____。