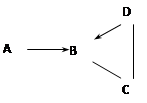��Ŀ����
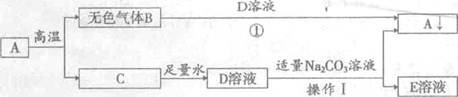
��7�֣�����֪ʶ������һ����Ҫ��ѧϰ��������ͼ�ǹ�������ѧ���ʵ�֪ʶ���磨��������ʾһ������ת��Ϊ��һ�����ʣ�������B���ܶ���С�����壬CΪ��ɫ���嵥�ʡ���ش��������⣺
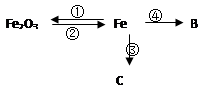
��1��C���ʵĻ�ѧʽΪ ��
��2��B���ʵ�һ����;�� ��
��3����Ӧ�ڻ���Ҫ��һ�ַ�Ӧ���� ���ѧʽ����
��4��д���ܷ�Ӧ�Ļ�ѧ����ʽ�� ��
��5����Ӧ�ٵ���ÿ���д����ĸ�����ʴ��Ϊ��ֹ�÷�Ӧ�ķ��������dz������ڸ�������Ϳˢ�����������������ȷ����������ַ����Ĺ�ͬԭ������ֹ������ �Ӵ���
��6���г��ϳ��۵IJ�Ѫ��Ƭ�г�����������ϸС�Ļ�ԭ�����ۣ�����������θҺ�е�
������Ӧת��Ϊ�Ȼ���������Ѫ�����á�
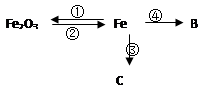
��1��C���ʵĻ�ѧʽΪ ��
��2��B���ʵ�һ����;�� ��
��3����Ӧ�ڻ���Ҫ��һ�ַ�Ӧ���� ���ѧʽ����
��4��д���ܷ�Ӧ�Ļ�ѧ����ʽ�� ��
��5����Ӧ�ٵ���ÿ���д����ĸ�����ʴ��Ϊ��ֹ�÷�Ӧ�ķ��������dz������ڸ�������Ϳˢ�����������������ȷ����������ַ����Ĺ�ͬԭ������ֹ������ �Ӵ���
��6���г��ϳ��۵IJ�Ѫ��Ƭ�г�����������ϸС�Ļ�ԭ�����ۣ�����������θҺ�е�
������Ӧת��Ϊ�Ȼ���������Ѫ�����á�
��7�֣�
��1�� Cu ��2�� ��ȼ�ϣ��������ᡢ���������
��3�� C����CO����H2�Ȼ�ԭ����
��4�� Fe + 2HCl = FeCl2 + H2������Fe + H2SO4 = FeSO4 + H2����
��5�� ���� ��6�� ���ᣨ��HCl��
��1�� Cu ��2�� ��ȼ�ϣ��������ᡢ���������
��3�� C����CO����H2�Ȼ�ԭ����
��4�� Fe + 2HCl = FeCl2 + H2������Fe + H2SO4 = FeSO4 + H2����
��5�� ���� ��6�� ���ᣨ��HCl��
�������ܶ���С������Ϊ������������BΪ���������ת����ϵͼ������ת���ɺ�ɫ���嵥��CΪͭ��Ȼ��������ʵ����ʺͷ�Ӧ���ɽ�����գ�
�⣺��1��C�����Ǻ�ɫ���壬������ת����������ôC����ͭ����ѧʽΪ Cu��
��2��B�������ܶ���С�����壬���������������п�ȼ�Ժ��ܶ�С�����ʣ�����һ����;�� ��ȼ�ϣ��������ᡢ���������
��3������������Ϊ������Ҫ��ԭ���������� C����CO����H2�Ȼ�ԭ������
��4�������ᷴӦ������������ѧ����ʽΪ��Fe+2HCl=FeCl2+H2������Fe+H2SO4=FeSO4+H2������
��5�����ݸ�����������������dz������ڸ�������Ϳˢ�����������������ȷ�������ֹ�����⣬�����ַ����Ĺ�ͬԭ������ֹ����������Ӵ���
��6������������θҺ�е� ���ᷢ����Ӧת��Ϊ�Ȼ���������Ѫ�����ã�
�ʴ�Ϊ����1��Cu
��2����ȼ�ϣ��������ᡢ���������
��3��C����CO����H2�Ȼ�ԭ����
��4��Fe+2HCl=FeCl2+H2������Fe+H2SO4=FeSO4+H2����
��5������
��6������
�⣺��1��C�����Ǻ�ɫ���壬������ת����������ôC����ͭ����ѧʽΪ Cu��
��2��B�������ܶ���С�����壬���������������п�ȼ�Ժ��ܶ�С�����ʣ�����һ����;�� ��ȼ�ϣ��������ᡢ���������
��3������������Ϊ������Ҫ��ԭ���������� C����CO����H2�Ȼ�ԭ������
��4�������ᷴӦ������������ѧ����ʽΪ��Fe+2HCl=FeCl2+H2������Fe+H2SO4=FeSO4+H2������
��5�����ݸ�����������������dz������ڸ�������Ϳˢ�����������������ȷ�������ֹ�����⣬�����ַ����Ĺ�ͬԭ������ֹ����������Ӵ���
��6������������θҺ�е� ���ᷢ����Ӧת��Ϊ�Ȼ���������Ѫ�����ã�
�ʴ�Ϊ����1��Cu
��2����ȼ�ϣ��������ᡢ���������
��3��C����CO����H2�Ȼ�ԭ����
��4��Fe+2HCl=FeCl2+H2������Fe+H2SO4=FeSO4+H2����
��5������
��6������

��ϰ��ϵ�д�
�����Ŀ