题目内容
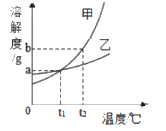
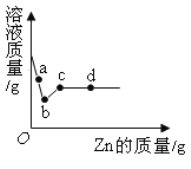
【题目】向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入过量Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如图所示.
(1)写出![]() (不包括b点)段反应的化学方程式_______.
(不包括b点)段反应的化学方程式_______.
(2)分别写出a、d所对应溶质的化学式_______。
(3)指出a~ b段溶液质量变化的原因_______。
【答案】Zn + Cu(NO3)2 == Zn(NO3)2 + Cu a: AgNO3 、Cu(NO3)2 、Zn(NO3)2 d: Zn(NO3)2 参加反应AgNO3的质量大于生成Zn(NO3)2的质量
【解析】
(1)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn时,锌先和硝酸银反应生成硝酸锌和银,后和硝酸铜反应生成硝酸锌和铜,反应的化学方程式及其质量关系为:
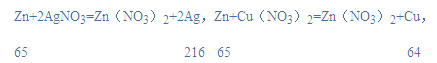
由以上质量关系可知,锌和硝酸银反应时溶液质量减小,和硝酸铜反应时溶液质量增大,a点时锌和部分硝酸银反应,溶液中的溶质有反应生成的硝酸锌、没有反应的硝酸铜和过量的硝酸银;
b~c段反应后溶液质量增大,是锌和硝酸铜反应,反应的化学方程式为:Zn+Cu(NO3)2═Zn(NO3)2+Cu;
(2)在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是三种;c点时硝酸铜恰好完全反应,溶液中只有硝酸锌,则d点的溶质为硝酸锌;
(3)a~b段溶液中,锌和硝酸银反应生成硝酸锌和银,由方程式可知,溶液的质量一直减小。

【题目】下列实验中,相关实验现象的描述错误的是
镁条在空气中燃烧 |
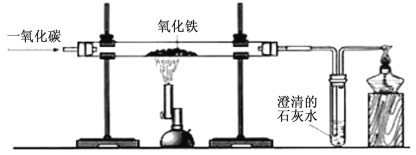
测定空气中氧气含量 |
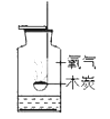
木炭在氧气中燃烧 |
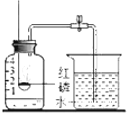
CO2通入石蕊试液中 |
A、产生耀眼的白光、生成黑色固体 | B、产生大量白烟;集气瓶内液面上升约至刻度“1” | C、发白光、石灰水变浑浊 | D、紫色石蕊试液变红色 |
A. AB. BC. CD. D