题目内容
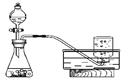
【题目】通过实验现象和题给信息,按要求填空。为测定空气的成分按下图进行实验: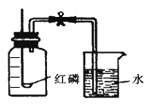
(1)将燃烧匙中过量的红磷点燃后放集气瓶中,此时能观察到的现象是_______________________,反应的化学方程式是:______________。
(2)此实验的结论是____________________________________。
(3)此实验进入集气瓶的水超过第一个刻度线的原因是___________(答一条)
(4)已知:镁+氮气 点燃→氮化镁(固体) 根据上述反应,能否用镁来测定空气中氮气所占的体积分数?____(填“能”或“不能”)
【答案】 红磷燃烧,产生大量白烟 略 O2约占空气总体积的五分之一 弹簧夹未夹紧(或塞瓶塞时速度太慢 不能
【解析】(1)红磷燃烧产生大量白烟,放出热量,生成物是五氧化二磷,反应的化学方程式为:4P+5O2![]() 2P2O5; (2)反应后冷却打开止水夹,烧杯中的水会进入达到集气瓶体积的五分之一,故结论:O2约占空气总体积的五分之一;(3) 此实验进入集气瓶的水超过第一个刻度线,是因为实验过程中瓶内的气体排出的过多导致的,造成的原因可能是弹簧夹未夹紧或塞瓶塞时速度太慢; (4)镁在空气中燃烧即与氧气反应,又与氮气反应,整个装置会进满水,故不能镁测定空气中氮气所占的体积分数。
2P2O5; (2)反应后冷却打开止水夹,烧杯中的水会进入达到集气瓶体积的五分之一,故结论:O2约占空气总体积的五分之一;(3) 此实验进入集气瓶的水超过第一个刻度线,是因为实验过程中瓶内的气体排出的过多导致的,造成的原因可能是弹簧夹未夹紧或塞瓶塞时速度太慢; (4)镁在空气中燃烧即与氧气反应,又与氮气反应,整个装置会进满水,故不能镁测定空气中氮气所占的体积分数。

练习册系列答案
相关题目