题目内容
【题目】(1)甲、乙、丙三种固体的溶解度曲线如图所示,据图回答:
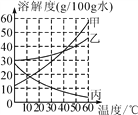
①30 ℃时,丙的溶解度是____;
②50 ℃时,在100 g水中放入50 g乙物质,充分搅拌后所得溶液的溶质质量分数为____(计算结果保留至0.1%);
③若将20 ℃时甲、乙、丙三种物质的饱和溶液升温至40 ℃(不考虑水的蒸发),可析出晶体的是____;
④将50 ℃时甲、乙、丙三种物质的饱和溶液均降温至10 ℃,所得溶液的溶质质量分数从大到小的顺序是____。
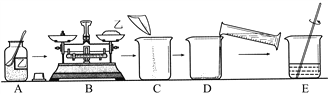
(2)常温下欲配置100 g溶质质量分数为10%的乙溶液,操作如图所示。
请回答下列问题:
①图中操作有错误的是____(填对应字母)。
②量取水时,若采用仰视的方法读数,会导致所配溶液的溶质质量分数____(填“偏大”“偏小”或“无影响”)。
【答案】 10_g 28.6% 丙 乙、甲、丙 B 偏小
【解析】(1)①据图可以看出,30℃时,丙的溶解度是10g;
②50℃时,乙物质的溶解度是40g,在100g水中放入50g乙物质,充分搅拌后,只能溶解40g,故所得溶液的溶质质量分数为![]() ×100%≈28.6%;
×100%≈28.6%;
③若将20℃时甲、乙、丙三种物质的饱和溶液升温至40℃,丙的溶解度随温度的升高而减小,故可析出晶体的是丙;
④将50℃时甲、乙、丙三种物质的饱和溶液均降温至10℃,甲和乙都会析出晶体,形成的仍然是饱和溶液,且乙的溶解度大于甲,故乙溶液的溶质质量分数大于甲,而丙的溶解度随温度的降低而增大,溶液组成不变,据图可以看出,丙的溶质质量分数小于甲,故所得溶液的溶质质量分数从大到小的顺序是乙>甲>丙;
(2)①称量物质时要左物右码,故图中操作有错误的是B;
②量取水时,若采用仰视的方法读数,则水会增大,故会导致所配溶液的溶质质量分数偏小。

练习册系列答案
相关题目