题目内容
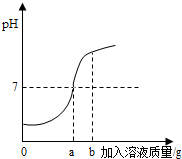 在用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.
在用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.(1)该实验是将
(2)当加入溶液的质量为bg时,所得溶液中的溶质为(写化学式)
(3)请列举一种中和反应在实际中的应用
考点:中和反应及其应用,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:(1)根据图象中pH值的变化是从小于7逐渐的增大到大于7,进行分析确定操作的过程;
(2)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,说明氢氧化钠溶液过量;
(3)酸性物质和碱性物质混合,能发生酸碱中和反应.
(2)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,说明氢氧化钠溶液过量;
(3)酸性物质和碱性物质混合,能发生酸碱中和反应.
解答:(1)由图象可知,pH值是开始时小于7逐渐的增大到7然后大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH升高,说明是把氢氧化钠溶液滴加到稀硫酸中;
(2)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,说明氢氧化钠溶液过量,此时所得溶液中的溶质为反应生成的硫酸钠和过量的氢氧化钠;
(3)可用熟石灰改良酸性土壤,氢氧化镁治疗胃酸过多是中和反应在实际中的应用.
故答案为:(1)氢氧化钠溶液;
(2)Na2SO4 NaOH;
(3)可用熟石灰改良酸性土壤,氢氧化镁治疗胃酸过多
(2)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,说明氢氧化钠溶液过量,此时所得溶液中的溶质为反应生成的硫酸钠和过量的氢氧化钠;
(3)可用熟石灰改良酸性土壤,氢氧化镁治疗胃酸过多是中和反应在实际中的应用.
故答案为:(1)氢氧化钠溶液;
(2)Na2SO4 NaOH;
(3)可用熟石灰改良酸性土壤,氢氧化镁治疗胃酸过多
点评:本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
有些不法商贩把伪造的铜币进行生锈处理,然后当作古钱币贩卖,从中获取暴利.以下关于铜生锈的过程的说法正确的是( )
| A、只不过是一种表面处理的过程 |
| B、是一种氧化反应过程 |
| C、铜本身没有发生变化 |
| D、应属于一种物理变化过程 |