题目内容
【题目】将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是 ( )
A.CaCl2 HCl NaNO3 B.KOH HCl (NH4)2SO4
C.K2CO3 Ba (NO3)2 NaOH D.FeCl3 NaCl KNO3
【答案】A
【解析】
试题分析:要使得大量共存且得到无色透明溶液,表明该物质彼此间不会反应。A选项设计的四种物质不会彼此反应,它们也均溶于水;B选项中KOH均能与HCl、(NH4)2SO4反应,所以无法大量共存;C选项中K2CO3 和Ba (NO3)2能相互反应生成白色沉淀,故它们不能大量共存;D选项中FeCl3是有颜色的,Fe3+是浅黄色的。故选择答案A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】空气中氧气含量测定的再认识.【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.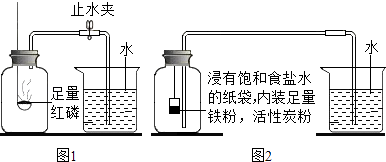
(1)写出红磷燃烧的化学方程式 .
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
(3)【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.【实验改进】
Ⅰ.根据铁在空气中生镑的原理设计图2验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
【交流表达】①铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式 .
②根据上表数据计算,改进实验后测得的空气中氧气的体积分数是(计算结果精确到0.1%).
(4)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:①;
② .
(5)【交流表达】①铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],该反应的化学方程式为:2Fe+O2+2H2O=2Fe(OH)2 . 故填:2Fe+O2+2H2O=2Fe(OH)2 . ②改进实验后测得的空气中氧气的体积分数为: ![]() ×100%=20.2%,故填:20.2%.从实验原理角度分析,改进后的实验结果比前者精确度更高的原因是:氧气完全反应,避免了燃烧匙伸入集气瓶中时导致的空气外逸.故填:氧气完全反应;避免了燃烧匙伸入集气瓶中时导致的空气外逸.
×100%=20.2%,故填:20.2%.从实验原理角度分析,改进后的实验结果比前者精确度更高的原因是:氧气完全反应,避免了燃烧匙伸入集气瓶中时导致的空气外逸.故填:氧气完全反应;避免了燃烧匙伸入集气瓶中时导致的空气外逸.