题目内容
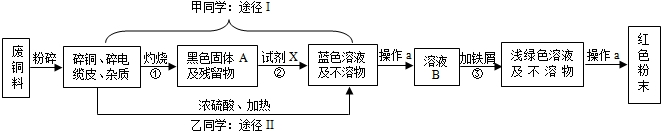
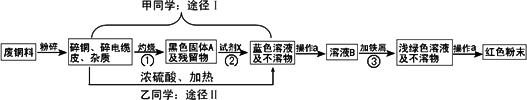
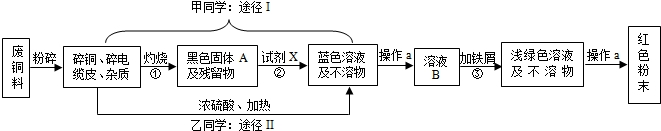
南洋电缆是汕头市一家以生产电缆类产品为主的上市公司.在电缆生产过程中,不可避免的会产生一定量的含铜废料(如:零碎电缆).金山中学化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.甲、乙同学根据已学知识,提出了两种途径: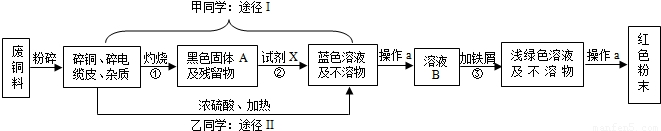
(1)A的化学式为,操作a的名称是.
(2)①的反应基本类型为;反应②、③的化学反应方程式分别是:
②;③.
(3)已知:Cu+2H2SO4 (浓)
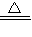 CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为(填I”或“Ⅱ”)的方案更合理.理由是:.
CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为(填I”或“Ⅱ”)的方案更合理.理由是:.(4)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应加入略过量的铁屑.丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?”.请提出一种简单的化学方法进行处理(用文字叙述):.
【答案】分析:“从含铜废料中回收铜”符合绿色化学的理念,再回收利用中,设计了两套方案,处理有关问题,并进行评价.甲方案中:发生的有关化学方程式为:①2Cu+O2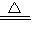 2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;
2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;
解答:解:(1)由题意,甲方案中:发生的有关化学方程式为:2Cu+O2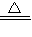 2CuO;所以黑色固体是氧化铜,操作a是分离固体与液体采用过滤的方法完成.
2CuO;所以黑色固体是氧化铜,操作a是分离固体与液体采用过滤的方法完成.
(2)①是发生的2Cu+O2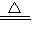 2CuO反应,是化合反应;
2CuO反应,是化合反应;
其中的反应主要有②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.
(3)从环保的角度,乙方案更合理,甲方案的“灼烧”会产生污染空气的气体、粉尘、烟雾;
(4)加入略过量的铁屑的目的是“确保CuSO4用完”或“将Cu完全置换出来“过量的铁粉可用酸液除掉.
故本题答案为:
(1)CuO;过滤.
(2)化合反应;CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.
(3)I.甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾.
(4)过滤前在加适量的酸以除去剩余的铁粉..
点评:本题探讨了“从含铜废料中回收铜”的有关问题,设计了不同的方案,并进行评价,考察了考生的思考、探讨、评价等诸多能力.
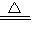 2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;
2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;解答:解:(1)由题意,甲方案中:发生的有关化学方程式为:2Cu+O2
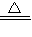 2CuO;所以黑色固体是氧化铜,操作a是分离固体与液体采用过滤的方法完成.
2CuO;所以黑色固体是氧化铜,操作a是分离固体与液体采用过滤的方法完成.(2)①是发生的2Cu+O2
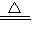 2CuO反应,是化合反应;
2CuO反应,是化合反应;其中的反应主要有②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.
(3)从环保的角度,乙方案更合理,甲方案的“灼烧”会产生污染空气的气体、粉尘、烟雾;
(4)加入略过量的铁屑的目的是“确保CuSO4用完”或“将Cu完全置换出来“过量的铁粉可用酸液除掉.
故本题答案为:
(1)CuO;过滤.
(2)化合反应;CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu.
(3)I.甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾.
(4)过滤前在加适量的酸以除去剩余的铁粉..
点评:本题探讨了“从含铜废料中回收铜”的有关问题,设计了不同的方案,并进行评价,考察了考生的思考、探讨、评价等诸多能力.

练习册系列答案
相关题目
 CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为______(填I”或“Ⅱ”)的方案更合理.理由是:______.
CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为______(填I”或“Ⅱ”)的方案更合理.理由是:______.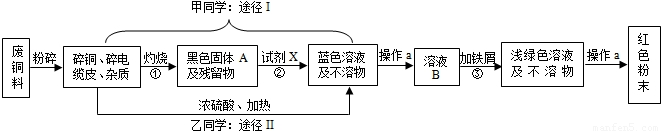
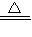 CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为 (填I”或“Ⅱ”)的方案更合理.理由是: .
CuSO4+SO2↑+2H2O.从环保角度对两种途径的不同部分进行比较,你认为 (填I”或“Ⅱ”)的方案更合理.理由是: .