题目内容
【题目】t℃测得某物质(不含结晶水)在不同质量的水中溶解达到饱和状态时所溶解该物质的质量,绘制成如图中斜线。下列说法错误的是( )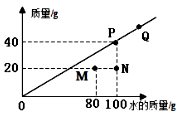
A.t℃时该物质的溶解度为40g
B.N点表示溶液中溶质的质量分数为20%
C.加溶质能使M点的溶液达到饱和状态
D.图中4点表示的溶液中溶质质量分数的关系是:N<M<P=Q
【答案】B
【解析】A.由图示可知t℃时该物质的溶解度为40g,A不符合题意;
B.N点表示100g水中溶解20g溶质,溶液中溶质的质量分数为 ![]() ≠20%,B符合题意;
≠20%,B符合题意;
C.M点为80g水中溶解了20克溶质,此时溶液为不饱和溶液,添加溶质能使M点的溶液达到饱和状态,C不符合题意;
D.P、Q均是这一温度的饱和溶液故此溶液溶质质量分数相等,M与N溶质是相同的而溶剂不同,可判断出N<M,由于温度相同时不饱和溶液最浓,可知它们的关系是:N<M<P=Q,D不符合题意;
所以答案是:B。
【考点精析】通过灵活运用固体溶解度曲线及其作用和溶质的质量分数,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质的质量分数=(溶质质量/溶液质量)*100% = [溶质质量/(溶质质量+溶剂质量]*100%即可以解答此题.

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案【题目】在化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂,为了确定其成分,同学们进行了如下的探究活动:
【查阅资料】
Ⅰ.石灰干燥剂的有效成分为生石灰(CaO)
Ⅱ.Ca(OH)2是一种微溶于水的白色固体,其水溶液(俗称石灰水)具有如下性质:能使无色酚酞(一种化学指示剂)溶液变红,与CO2气体反应出现浑浊,能与盐酸反应但无明显现象。
【方案设计】
小组成员设计了如下实验方案以期得到相应推论:取样滴加稀盐酸,有气泡产生,则白色固体为CaCO3;若无气泡产生,则白色固体为Ca(OH)2
(1)请简要说明上述方案中不合理之处:___________。
(2)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你设计一种实验方案予以证明。
实验步骤 | 实验现象 | 结论 |
______________ | _____________ | 含CaCO3 |
______________ | _____________ | 含Ca(OH)2 |
【数据分析】
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学向10克样品中加入足量的稀盐酸,测得CO2气体的质量如图所示。
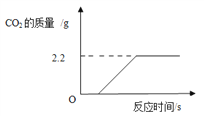
(3)根据题给信息猜想一下,实验开始时的一段时间没有CO2气体产生的原因是_______;计算该混合物中CaCO3的质量分数_____________(请写出过程)。
【反思与评价】
实验中,如有部分二氧化碳气体因溶解于水而没有全部逸出,则测得的混合物中CaCO3的质量分数________(填写“偏大”、 “偏小”或“不变”)。