题目内容
【题目】在氧化镁和碳酸镁的混合物12.4g,加入100g质量分数为14.6%的稀盐酸,恰好完全反应,则加入稀盐酸生成气体的质量( )
A. 2.2g B. 4.4g C. 3.3g D. 1.1g
【答案】B
【解析】
解:设混合物中氧化镁的质量为m,则碳酸镁的质量为:12.4g-m;设氧化镁消耗的氯化氢的质量为x,碳酸镁消耗的氯化氢的质量为y,
MgO+2HCl=MgCl2+H2O
40 73
m x
![]() x=
x=![]() ,
,
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 73
12.4g-m y
![]() y=
y=![]() ,
,
![]() +
+![]() =100g×14.6%,m=4g;则混合物中含碳酸镁的质量为:12.4g-4g=8.4,设8.4g碳酸镁与盐酸完全反应生成二氧化碳的质量为z,
=100g×14.6%,m=4g;则混合物中含碳酸镁的质量为:12.4g-4g=8.4,设8.4g碳酸镁与盐酸完全反应生成二氧化碳的质量为z,
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 44
8.4g z
z=4.4g。故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)高层建筑物通常设计了灭火用的洒水系统。从灭火原理分析,洒水的作用主要是_______________________。
(2)分析下表中的数据,回答问题:
物质代号 | L | M | N | P |
熔点/℃ | -117 | 3550 | 44 | -259 |
沸点/℃ | 78 | 4827 | 257 | -253 |
着火点/℃ | 510 | 370 | 40 | 580 |
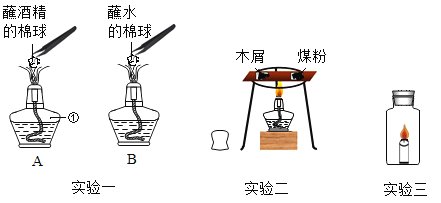
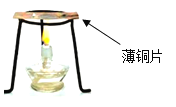
有人认为“物质的熔、沸点越高,着火点越高”,该结论_________(填 “合理”或“不合理”)。已知酒精灯火焰的温度约为500℃。利用如图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是________(填代号)。
【题目】石油是重要的地球资源。请回答下列相关问题:
(1)用石油可以精炼出多种燃料。根据下表分析,在相同条件下,柴油比汽油燃烧时更容易产生黑烟,原因是_____,造成的环境问题是_____。
汽油的主要成分 | C5H12、C6H14……C12H24 |
柴油的主要成分 | C14H22、C16H34……C18H38 |
(2)为了改善环境,可在汽油中添加乙醇(C2H5OH)来调整燃油结构。乙醇是_____(填“可再生”或”不可再生”)能源,其完全燃烧的化学方程式是_____。
(3)氢燃料汽车正在研制与推广。氢气燃烧时是将_____能转化成热能。从长远观点看,解决能源危机的方法是_____。
(4)合理利用石油资源,可制成多种合成材料。下列物品主要成分属于合成材料的是_____。
A.塑料水盆 B.羊绒围巾 C.橡胶足球 D.玻璃水杯