题目内容
(9分)盐酸和氯化坝的混合溶液40g,其中盐酸的溶质质量分数为10%.向混合溶液中加入9%的硫酸溶液20g恰好完全反应.计算:
(1)生成沉淀的质量是多少克?
(2)反应后所得溶液中盐酸的质量分数.(计算结果精确到0.1)
【答案】
(1)4.3g;(2)9.5%
【解析】
试题分析:
根据题意可以知道反应中消耗了硫酸的质量为:20g×9%=1.8g
设生成BaSO4沉淀的质量为x,生成HCl的质量为y
BaCl2+H2SO4═BaSO4↓+2HCl
98 233 73
1.8g x y
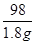 =
=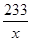 =
=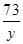
解得:x=4.3g y=1.3g
(2)所以反应后溶液中氯化氢的质量为:40g×10%+1.3g=5.3g
反应后溶液的质量为:40g+20g﹣4.3g=55.7g
反应后溶液中含HCl的质量分数为: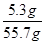 ×100%=9.5%;
×100%=9.5%;
答:(1)生成沉淀的质量是4.3克;
(2)反应后所得溶液中盐酸的质量分数9.5%
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算

练习册系列答案
相关题目