题目内容
在实验室配制石灰水时,小明同学将两药匙熟石灰样品放入小烧杯中,向其中加入一定量的蒸馏水,充分搅拌后发现烧杯底部仍有不溶性的固体,于是他认为熟石灰样品已经变质。小艳同学不同意他的判断,你认为小艳同学的理由是 。针对该熟石灰样品的成分同学们展开了讨论,请你参与讨论并完成实验报告。
【提出问题】熟石灰样品的主要成分是什么?
【作出猜想】甲同学猜想是Ca(OH)2;
乙同学猜想是CaCO3;
你认为是 。
【实验与结论】请你通过实验验证你的猜想:
【提出问题】熟石灰样品的主要成分是什么?
【作出猜想】甲同学猜想是Ca(OH)2;
乙同学猜想是CaCO3;
你认为是 。
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤。 向滤液中加入适量的 溶液; (2)向滤出固体中加入适量 。 | (1) ; (2) 。 | 猜想正确 |
氢氧化钙的溶解度很小或加水量不足;Ca(OH)2和CaCO3;
| (1)酚酞 | 酚酞溶液变红,说明样品中含有氢氧化钙; |
| (2)稀盐酸 | 有气泡冒出 |
试题分析:小艳同学的理由是:氢氧化钙的溶解度很小或加水量不足,这两种情况都可以导致不能形成澄清的溶液,故填:氢氧化钙的溶解度很小或加水量不足;
【作出猜想】
甲同学猜想是Ca(OH)2;乙同学猜想是CaCO3;你认为是Ca(OH)2和CaCO3;
【实验与结论】
取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤,向滤液中加入适量酚酞溶液,酚酞溶液变红,说明样品中含有氢氧化钙;向滤出固体中加入适量的稀盐酸,有气泡冒出,说明样品中含有碳酸钙;故填:酚酞;酚酞溶液变红;稀盐酸;有气泡冒出。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目

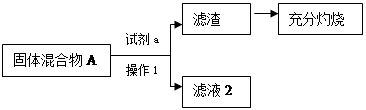
 (1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。
(1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。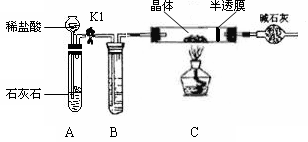
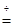 ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。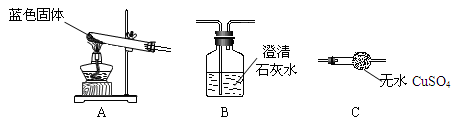
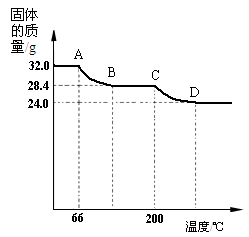



 三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。
三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。