��Ŀ����
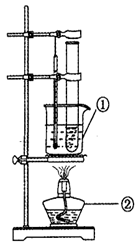
��5�֣���������(��ѧʽΪNa2O2)����CO2��Ӧ����ѧ����ʽΪ2Na2O2 + 2CO2 =" 2Na2CO3" + O2���������ں����������Ϊ������Դ��ijʵ��С�����ø���Ķ�����̼��������Ʒ�Ӧ�ռ�һƿ������ʵ��װ������ͼ��ʾ����ش����⡣

��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ �� ��
��Ũ����������� �� ��
����ʵ������з��ֳ����ʯ��ˮ����ǣ���ԭ�����Ϊ �� ��������Ӧ�Ļ�ѧ����ʽΪ
����������Eװ���ռ������ô����ǵ�ľ�����飬���������������� �� ����

��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ �� ��
��Ũ����������� �� ��
����ʵ������з��ֳ����ʯ��ˮ����ǣ���ԭ�����Ϊ �� ��������Ӧ�Ļ�ѧ����ʽΪ
����������Eװ���ռ������ô����ǵ�ľ�����飬���������������� �� ����
��CaCO3 + 2HCl =" CaCl2" + H2O + CO2��
�Ƹ��������̼��������ˮ�֣�
�Ƕ�����̼û�к���������ȫ��Ӧ Ca(OH)2 + CO2 = CaCO3��+ H2O
���ܶȱȿ�������֧��ȼ��
�Ƹ��������̼��������ˮ�֣�
�Ƕ�����̼û�к���������ȫ��Ӧ Ca(OH)2 + CO2 = CaCO3��+ H2O
���ܶȱȿ�������֧��ȼ��
��������1��������ȡ������̼�ķ�Ӧԭ��ֱ��д����Ӧ�ķ���ʽ��
��2��Ũ����ͨ������Ϊ�������ʹ�õģ�
��3�����ݷ�Ӧ�����ж�����̼�ܷ���ȫ���������
��4�������ܹ�֧��ȼ�գ�
��𣺽⣺��1��ֱ��д��ʵ������ȡ������̼�Ļ�ѧ����ʽ��
��2��Ũ������Ϊ����������ն�����̼������ˮ������
��3��������̼�dz������ϵ�ͨ��Cװ���У��ض���һ������������Ӧ������Dװ�ã�
��4�������ܹ�֧��ȼ�����ܶȱȿ����Ĵ���ʹ�����ǵ�ľ����ȼ��
�ʴ�Ϊ����1��CaCO3+2HCl�TCaCl2+H2O+CO2��
��2�����������̼��������ˮ�֣�
��3��������̼û�к���������ȫ��Ӧ��Ca��OH��2+CO2=CaCO3��+H2O
��4���ܶȱȿ�������֧��ȼ��
��2��Ũ����ͨ������Ϊ�������ʹ�õģ�
��3�����ݷ�Ӧ�����ж�����̼�ܷ���ȫ���������
��4�������ܹ�֧��ȼ�գ�
��𣺽⣺��1��ֱ��д��ʵ������ȡ������̼�Ļ�ѧ����ʽ��
��2��Ũ������Ϊ����������ն�����̼������ˮ������
��3��������̼�dz������ϵ�ͨ��Cװ���У��ض���һ������������Ӧ������Dװ�ã�
��4�������ܹ�֧��ȼ�����ܶȱȿ����Ĵ���ʹ�����ǵ�ľ����ȼ��
�ʴ�Ϊ����1��CaCO3+2HCl�TCaCl2+H2O+CO2��
��2�����������̼��������ˮ�֣�
��3��������̼û�к���������ȫ��Ӧ��Ca��OH��2+CO2=CaCO3��+H2O
��4���ܶȱȿ�������֧��ȼ��

��ϰ��ϵ�д�
�����Ŀ







 �� ��ơ�ʵ��1����Ŀ���� ����
�� ��ơ�ʵ��1����Ŀ���� ���� ��I�� 2KClO3 + 2MnO2="==2KMnO4" + Cl2��+ O2����
��I�� 2KClO3 + 2MnO2="==2KMnO4" + Cl2��+ O2���� ��III��K2MnO4 + Cl2="==2KCl" + MnO2 + O2����
��III��K2MnO4 + Cl2="==2KCl" + MnO2 + O2����