题目内容
 化肥在提高粮食产量,解决人类吃饭问题上发挥重要作用.
化肥在提高粮食产量,解决人类吃饭问题上发挥重要作用.
(1)下列均为常见的化学肥料:
①碳酸氢铵(NH4HCO3)②尿素[CO(NH2)2]③硝酸钾KNO3 ④磷酸二氢钙[Ca(H2PO4)2].上述四种化肥中属于复合肥的是______(填序号);
①和②两种化肥相比较,N元素质量分数较低的是______(填序号).
(2)资料表明,在高温高压下以CO2和NH3为原料合成尿素[CO(NH2)2],同时有物质X生成,反应方程式可表示为:CO2+2NH3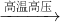 CO(NH2)2+X; X物质的化学式为______;在尿素中碳、氧、氮、氢元素的质量比为______.
CO(NH2)2+X; X物质的化学式为______;在尿素中碳、氧、氮、氢元素的质量比为______.
(3)小华同学的父亲买了一化肥,其包装袋上的一部分内容如图所示:
为了确定该化肥是否符合标准,小华同学称取20g样品(所含杂质不参加反应),加入一定质量的水全部溶解后与100g 氯化钡溶液恰好完全反应,经过滤,洗涤,干燥,得固体23.3g.请通过计算回答:
①该化肥是否符合标准.
②所用氯化钡溶液中溶质的质量分数.
解:(1)①碳酸氢铵(NH4HCO3)中只含营养元素中的氮元素,故是氮肥;②尿素[CO(NH2)2]中只含营养元素中的氮元素,故是氮肥;③硝酸钾KNO3 中含营养元素中的氮元素和钾元素,故是复合肥;④磷酸二氢钙[Ca(H2PO4)2]中只含营养元素中的磷元素,故是磷肥;
碳酸氢铵中氮元素的质量分数= ×100%=17.7%;尿素中氮元素的质量分数=
×100%=17.7%;尿素中氮元素的质量分数= ×100%=46.7%,故碳酸氢铵中的氮元素的质量分数低;
×100%=46.7%,故碳酸氢铵中的氮元素的质量分数低;
故答案为:③①;
(2)反应前有1个碳原子、2个氧原子、2个氮原子和6个氢原子,反应后出现1个碳原子、1个氧原子、2个氮原子和4个氢原子,根据反应前后原子的个数和种类都不变可知,缺少2个氢原子和1个氧原子存在1个X分子中,故X的化学式是:H2O;
[CO(NH2)2]中 碳、氧、氮、氢元素的质量比=12:16:14×2:1×4=3:4:7:1;
故答案为:H2O; 3:4:7:1;
(3)设生成2.33g沉淀需要硫酸钾的质量是X,氯化钡的质量是Y,
K2SO4+BaCl2=BaSO4↓+2KCl
174 208 233
X Y 23.3g
 =
=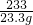 X=17.4g∴硫酸钾的质量分数=
X=17.4g∴硫酸钾的质量分数= ×100%=87%<95% 故不符合标准;
×100%=87%<95% 故不符合标准;
 =
=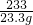 Y=20.8g∴氯化钡的质量分数=
Y=20.8g∴氯化钡的质量分数= ×100%=20.8%
×100%=20.8%
答:该化肥不符合标准,氯化钡的质量分数是20.8%.
分析:(1)复合肥是含有N、P、K中的两种或两种以上的肥料;根据化合物中某元素的质量分数公式计算;
(2)根据质量守恒定律中化学反应前后原子的种类和个数都不变分析X的化学式;元素的质量比等于个元素的原子个数×相对原子质量的比值;
(3)根据化学方程式的计算步骤分析:根据沉淀的质量求出硫酸钾的质量及氯化钡的质量,再根据质量分数的公式计算出硫酸钾和氯化钡的质量分数.
点评:本题考查了与农业生产有关的化学肥料判断、计算,难度不大,根据已有的知识逐一解决即可.
碳酸氢铵中氮元素的质量分数=
 ×100%=17.7%;尿素中氮元素的质量分数=
×100%=17.7%;尿素中氮元素的质量分数= ×100%=46.7%,故碳酸氢铵中的氮元素的质量分数低;
×100%=46.7%,故碳酸氢铵中的氮元素的质量分数低;故答案为:③①;
(2)反应前有1个碳原子、2个氧原子、2个氮原子和6个氢原子,反应后出现1个碳原子、1个氧原子、2个氮原子和4个氢原子,根据反应前后原子的个数和种类都不变可知,缺少2个氢原子和1个氧原子存在1个X分子中,故X的化学式是:H2O;
[CO(NH2)2]中 碳、氧、氮、氢元素的质量比=12:16:14×2:1×4=3:4:7:1;
故答案为:H2O; 3:4:7:1;
(3)设生成2.33g沉淀需要硫酸钾的质量是X,氯化钡的质量是Y,
K2SO4+BaCl2=BaSO4↓+2KCl
174 208 233
X Y 23.3g
 =
=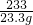 X=17.4g∴硫酸钾的质量分数=
X=17.4g∴硫酸钾的质量分数= ×100%=87%<95% 故不符合标准;
×100%=87%<95% 故不符合标准; =
=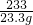 Y=20.8g∴氯化钡的质量分数=
Y=20.8g∴氯化钡的质量分数= ×100%=20.8%
×100%=20.8%答:该化肥不符合标准,氯化钡的质量分数是20.8%.
分析:(1)复合肥是含有N、P、K中的两种或两种以上的肥料;根据化合物中某元素的质量分数公式计算;
(2)根据质量守恒定律中化学反应前后原子的种类和个数都不变分析X的化学式;元素的质量比等于个元素的原子个数×相对原子质量的比值;
(3)根据化学方程式的计算步骤分析:根据沉淀的质量求出硫酸钾的质量及氯化钡的质量,再根据质量分数的公式计算出硫酸钾和氯化钡的质量分数.
点评:本题考查了与农业生产有关的化学肥料判断、计算,难度不大,根据已有的知识逐一解决即可.

练习册系列答案
相关题目
 化肥在提高粮食产量,解决人类吃饭问题上发挥重要作用.
化肥在提高粮食产量,解决人类吃饭问题上发挥重要作用. 粮食问题一直困扰着人类,1824年,德国化学家维勒首次人工合成尿素,标志着化学肥料的诞生.之后化肥参全世界普遍应用,使粮食产量大幅度增长.
粮食问题一直困扰着人类,1824年,德国化学家维勒首次人工合成尿素,标志着化学肥料的诞生.之后化肥参全世界普遍应用,使粮食产量大幅度增长.