题目内容
5.6 g铁跟足量的稀硫酸起反应,可制得氢气多少克?(Fe+H2SO4═FeSO4+H2↑)
解:设生成氢气的质量为x.
Fe+H2SO4═FeSO4+H2↑
56 2
5.6g x
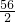 =
=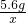 ,x=0.2g
,x=0.2g
答:可制得氢气0.2g.
分析:由铁的质量根据铁与硫酸反应的化学方程式可以计算出生成氢气的质量.
点评:本题主要考查有关化学方程式的计算,难度较小.
Fe+H2SO4═FeSO4+H2↑
56 2
5.6g x
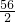 =
=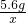 ,x=0.2g
,x=0.2g答:可制得氢气0.2g.
分析:由铁的质量根据铁与硫酸反应的化学方程式可以计算出生成氢气的质量.
点评:本题主要考查有关化学方程式的计算,难度较小.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目