题目内容
某校化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中3次检验的结果如下表所示.
阅读上表后回答:
(1)表中第
(2)为验证其他2次检验结果中是否存在SO42-、CO32-和Cl-,又进行以下操作:①加入过量的
(3)通过上述实验,该小组还是觉得无法确定其他2次检验结果中哪一次是正确的,你认为可能的原因是
| 序号 | 溶液中检验出的物质 |
| 1 | KCl、K2SO4、Na2CO3 |
| 2 | Na2SO4、BaCl2、K2CO3 |
| 3 | Na2SO4、KCl、K2CO3 |
(1)表中第
2
2
次结果肯定不准确.(2)为验证其他2次检验结果中是否存在SO42-、CO32-和Cl-,又进行以下操作:①加入过量的
硝酸
硝酸
(填物质名称,下同),目的是检验CO32-
CO32-
并将其除去;②加入(过量的)硝酸钡
(过量的)硝酸钡
溶液,过滤;③向滤液中加入硝酸银
硝酸银
溶液.该小组同学查阅资料后,发现可以利用焰色反应来确定溶液中存在的阳离子.(3)通过上述实验,该小组还是觉得无法确定其他2次检验结果中哪一次是正确的,你认为可能的原因是
因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已
因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已
.分析:(1)根据各种物质在溶液中能否共存进行分析;
(2)在检验氯离子时,我们可用硝酸银和稀硝酸;在检验硫酸根离子时,我们可用硝酸钡和稀硝酸;为了排除碳酸根离子的干扰,我们可以先加硝酸排除碳酸根离子的干扰.
(3)根据在溶液中溶质存在形式进行分析.
(2)在检验氯离子时,我们可用硝酸银和稀硝酸;在检验硫酸根离子时,我们可用硝酸钡和稀硝酸;为了排除碳酸根离子的干扰,我们可以先加硝酸排除碳酸根离子的干扰.
(3)根据在溶液中溶质存在形式进行分析.
解答:解:
(1))因氯化钡与硫酸钠、碳酸钾能生成硫酸钡、碳酸钡沉淀不能在同一溶液中共存,所以我们判断第2个方案是错误;
(2)为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子时,因在确定氯离子和硫酸根离子时,必须排除碳酸根离子的干扰,所以我们首先检验并除去碳酸根离子;所以我们首先加过量的硝酸,检验并除去碳酸根离子;在检验氯离子和硫酸根离子时,我们先检验氯离子,因硝酸银能跟硫酸根离子生成硫酸银,是一种沉淀干扰检验,所以我们先加过量的硝酸钡溶液,检验并除去硫酸根离子,最再用硝酸银来检验氯离子;
(3)无法确定其他两次检验结果哪次正确,因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已
故答案为:
(1)2;
(2)硝酸,CO32-;(过量的)硝酸钡,硝酸银;
(3)因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已.
(1))因氯化钡与硫酸钠、碳酸钾能生成硫酸钡、碳酸钡沉淀不能在同一溶液中共存,所以我们判断第2个方案是错误;
(2)为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子时,因在确定氯离子和硫酸根离子时,必须排除碳酸根离子的干扰,所以我们首先检验并除去碳酸根离子;所以我们首先加过量的硝酸,检验并除去碳酸根离子;在检验氯离子和硫酸根离子时,我们先检验氯离子,因硝酸银能跟硫酸根离子生成硫酸银,是一种沉淀干扰检验,所以我们先加过量的硝酸钡溶液,检验并除去硫酸根离子,最再用硝酸银来检验氯离子;
(3)无法确定其他两次检验结果哪次正确,因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已
故答案为:
(1)2;
(2)硝酸,CO32-;(过量的)硝酸钡,硝酸银;
(3)因为溶液中溶质存在的形态主要是离子,1、3中的离子组成是相同的,区别仅仅是呈现形式不同而已.
点评:在确定溶液的组成时,首先要保证所确定的溶液中的溶质必须保证能在同一溶液中共存,也就是所确定的溶质不能发生化学反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
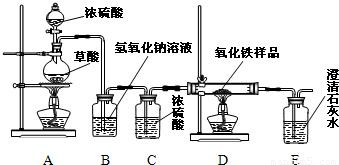
 某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4

 某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
某校化学课外兴趣小组的同学在研究性学习课展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应: CO↑+CO2↑+H2O
CO↑+CO2↑+H2O