题目内容
【题目】(5分)金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀。
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
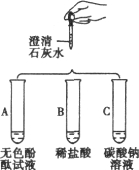
(3)用下列试剂验证铝、铁、铜这三种金属的活动性顺序,能达到目的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
(4)将等质量的锌粉和铁粉分别于溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示。请回答下列问题:
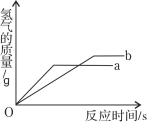
(1)表示铁粉与稀硫酸反应的曲线是: (填 a 或 b)
(2)对于曲线a表示的反应, (填化学式)有剩余。
【答案】(1)铝 (2)大 (3)B (4)b H2SO4
【解析】
试题分析:(1)铝在常温下易与空气中的氧气反应在表面形成一层致密的氧化物薄膜,故在空气中铝制品更耐腐蚀
(2)合金的抗腐蚀性比组成金属要更强,硬度要更大,熔点要更低,钢是铁的合金,故钢比纯铁硬度大
(3) 验证铝、铁、铜这三种金属的活动性顺序,可采用“两金夹一盐”(两种金属、一种盐溶液)或“两盐夹一金” (一种金属、两种盐溶液),故能达到目的是B
(4)根据金属的活动性:锌>铁,金属的活动性越强,反应速率就越快,故表示铁粉与稀硫酸反应的曲线是:b;根据图像,最终两种金属与酸反应产生的氢气质量不相等,说明对于曲线a表示的反应,H2SO4有剩余

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目