题目内容
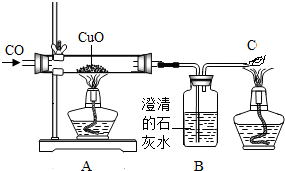 观察用CO还原CuO实验装置,回答:
观察用CO还原CuO实验装置,回答:(1)加热A处酒精灯前先通一氧化碳的目的
(2)实验现象
(3)导管尾部酒精灯的目的
(4)实验结束时应先
考点:一氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:(1)根据一氧化碳是一种可燃性的气体,与空气的混合气体在加热时易发生爆炸分析;
(2)一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳和石灰水的主要成分氢氧化钙反应生成碳酸钙和水,CO可燃进行分析解答;
(3)一氧化碳有毒,为防止污染大气,所以可以用燃烧的方法将其处理掉;
(4)实验结束后应先停止加热,待玻璃管冷却后再停止通一氧化碳气体.若这两个操作次序颠倒了,生成的铜在高温条件下又被进入的氧气氧化为氧化铜.
(2)一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳和石灰水的主要成分氢氧化钙反应生成碳酸钙和水,CO可燃进行分析解答;
(3)一氧化碳有毒,为防止污染大气,所以可以用燃烧的方法将其处理掉;
(4)实验结束后应先停止加热,待玻璃管冷却后再停止通一氧化碳气体.若这两个操作次序颠倒了,生成的铜在高温条件下又被进入的氧气氧化为氧化铜.
解答:解:(1)若不先通一氧化碳气体,排净玻璃管中的空气,由于该装置中混有空气,一氧化碳是可燃气体,如果和空气混合达到一定的极限,就可以爆炸;
(2)在A处观察到的现象是:黑色的氧化铜在高温条件下可以被一氧化碳还原为红色的铜,同时产生二氧化碳气体,二氧化碳和石灰水的主要成分氢氧化钙反应生成不溶于水的碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,一氧化碳尾气燃烧时发出蓝色火焰;
(3)一氧化碳有毒,为防止污染大气,所以可以用燃烧的方法将其处理掉;
(4)实验结束时应先熄灭加热氧化铜的酒精灯,继续通入CO至被还原的铜冷却,否则还原出的铜又会被空气中的氧气氧化;
故答案为:(1)排出装置中的空气,防止加热时发生爆炸;
(2)A处黑色粉末变红色,B处澄清的石灰水变浑浊,C处气体燃烧发出蓝色火焰;CO2+Ca(OH)2=CaCO3↓+H2O;
(3)除去尾气中的一氧化碳,防止污染空气;
(4)熄灭A处酒精灯;CO(或一氧化碳);防止还原后的单质铜被空气中的氧气氧化.
(2)在A处观察到的现象是:黑色的氧化铜在高温条件下可以被一氧化碳还原为红色的铜,同时产生二氧化碳气体,二氧化碳和石灰水的主要成分氢氧化钙反应生成不溶于水的碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O,一氧化碳尾气燃烧时发出蓝色火焰;
(3)一氧化碳有毒,为防止污染大气,所以可以用燃烧的方法将其处理掉;
(4)实验结束时应先熄灭加热氧化铜的酒精灯,继续通入CO至被还原的铜冷却,否则还原出的铜又会被空气中的氧气氧化;
故答案为:(1)排出装置中的空气,防止加热时发生爆炸;
(2)A处黑色粉末变红色,B处澄清的石灰水变浑浊,C处气体燃烧发出蓝色火焰;CO2+Ca(OH)2=CaCO3↓+H2O;
(3)除去尾气中的一氧化碳,防止污染空气;
(4)熄灭A处酒精灯;CO(或一氧化碳);防止还原后的单质铜被空气中的氧气氧化.
点评:明确一氧化碳还原氧化铜的实验爆炸、注意事项,物质的性质即可顺利解答.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
 为控制温室气体的排放,阿根廷科学家研发了一款放在牛身上的“放屁背包”(见右图),能够将牛屁排放的甲烷气体收集起来转化成汽车燃料.(一头重约544公斤的牛,每天放屁可释出800至1000公升甲烷,而甲烷的温室效应约是CO2的20倍以上).
为控制温室气体的排放,阿根廷科学家研发了一款放在牛身上的“放屁背包”(见右图),能够将牛屁排放的甲烷气体收集起来转化成汽车燃料.(一头重约544公斤的牛,每天放屁可释出800至1000公升甲烷,而甲烷的温室效应约是CO2的20倍以上). 毛毛跟你一样,刚学习了有关化学式量的计算.右图为毛毛服用的钙片的标签,老师用它编写了一道有关相对分子质量的计算题,请你跟他一起检验一下自己学习的情况吧.
毛毛跟你一样,刚学习了有关化学式量的计算.右图为毛毛服用的钙片的标签,老师用它编写了一道有关相对分子质量的计算题,请你跟他一起检验一下自己学习的情况吧. 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯上灼烧后迅速插入大试管,接触试管底部过量的白磷(化学式:P)引燃白磷,然后立即塞紧橡皮塞.可观察到大试管中产生大量的白烟.试回答以下问题:
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯上灼烧后迅速插入大试管,接触试管底部过量的白磷(化学式:P)引燃白磷,然后立即塞紧橡皮塞.可观察到大试管中产生大量的白烟.试回答以下问题: