题目内容
)回收的废旧锌锰于电池经过处理后得到锰粉(含MnO2、Mn(OH)2、Fe、乙炔和黑炭等),由锰粉制取MnO2的步骤如下图所示。

根据上图所示步骤并参考表格数据,回答下列问题。
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等。MnO2与浓盐酸反应的离子方程式为________________________________。
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是__________________________。
(3)过滤I所得滤液经氧化后,需加入NaOH溶
液调节pH约为5.1,其目的是______________________________________。
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离于方程式为__________________________________________。
(5)实验室进行过滤操作时.需要用到的玻璃仪器有___________________________。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


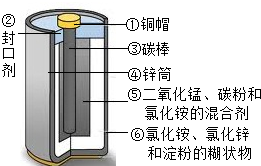
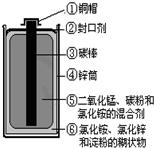 18、电池是一种把化学能转变为电能的装置.目前,废旧电池对环境的污染已越来越引起人们的重视.为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术.右图为普通电池(锌锰电池)示意图,请你根据图示分析:
18、电池是一种把化学能转变为电能的装置.目前,废旧电池对环境的污染已越来越引起人们的重视.为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术.右图为普通电池(锌锰电池)示意图,请你根据图示分析: (2010?丹东)目前,废旧电池对环境的污染已越来越引起人们的重视.为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术.右图为普通电池(锌锰电池)示意图,请你根据图示分析:
(2010?丹东)目前,废旧电池对环境的污染已越来越引起人们的重视.为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术.右图为普通电池(锌锰电池)示意图,请你根据图示分析: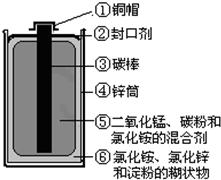 16、化学与生活有密切的联系,请完成下列问题:
16、化学与生活有密切的联系,请完成下列问题: