题目内容
(2006?镇江)如图是一些常见物质间互相转化的关系图(有些反应条件未注明)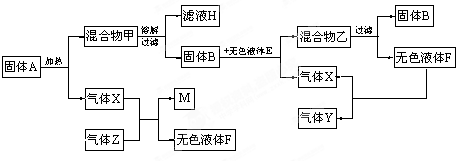
(1)将固体A充分加热至不再产生气体,滤液H中所含有的物质有:
(2)固体B的化学式为
(3)如果气体Z是最简单的有机物,它在气体X中燃烧,会因X的量的变化和条件的不同而生成不同的物质.试写出X和Z反应生成固体单质M和无色液体F的化学方程式:

(1)将固体A充分加热至不再产生气体,滤液H中所含有的物质有:
K2MnO4、H2O
K2MnO4、H2O
(写化学式)(2)固体B的化学式为
MnO2
MnO2
,它在与无色液体E的反应中起催化
催化
作用.(3)如果气体Z是最简单的有机物,它在气体X中燃烧,会因X的量的变化和条件的不同而生成不同的物质.试写出X和Z反应生成固体单质M和无色液体F的化学方程式:
CH4+O2
C+2H2O.
| ||
CH4+O2
C+2H2O.
.
| ||
分析:根据题意和框图信息,气体Z是最简单的有机物,则z是甲烷,根据加热固体A得到气体x和混合物,甲烷能在x中燃烧,则可推出固体A是高锰酸钾,x氧气,高锰酸钾受热分解生成的锰酸钾能溶于水,二氧化锰不溶于水,二氧化锰能加快过氧化氢分解放出氧气的速率.根据质量守恒定律分析,甲烷在氧气中燃烧时生成的固体和无色的液体,由此,可推出各物质,写出反应的方程式.
解答:解:(1)由题意题意和框图信息,气体Z是最简单的有机物,则z是甲烷,由加热固体A得到气体x和混合物,甲烷能在x中燃烧,则可推出固体A是高锰酸钾,x氧气,加热高锰酸钾至不再产生气体,残留物锰酸钾和二氧化锰,加水溶解过滤,滤液H中所含有的物质有K2MnO4、H2O;
(2)加热高锰酸钾生成的二氧化锰不溶于水,所以固体B是二氧化锰,化学式:MnO2,MnO2能催化过氧化氢分解放出氧气的速率;
(3)甲烷在燃烧时,如果氧气的量不足,则会生成固体单质M和无色液体F,由质量守恒定律可知,固体单质M应是碳,无色的液体应是水,反应的方程式是:CH4+O2
C+2H2O.
故答为:(1)K2MnO4、H2O;(2)MnO2,催化;(3)CH4+O2
C+2H2O.
(2)加热高锰酸钾生成的二氧化锰不溶于水,所以固体B是二氧化锰,化学式:MnO2,MnO2能催化过氧化氢分解放出氧气的速率;
(3)甲烷在燃烧时,如果氧气的量不足,则会生成固体单质M和无色液体F,由质量守恒定律可知,固体单质M应是碳,无色的液体应是水,反应的方程式是:CH4+O2
| ||
故答为:(1)K2MnO4、H2O;(2)MnO2,催化;(3)CH4+O2
| ||
点评:本题为物质的推断题,完成此类题目,可以依据题干提供的信息,结合转变关系,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 (2006?镇江)能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响.这就迫切要求人们开发氢能、太阳能等新能源.
(2006?镇江)能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响.这就迫切要求人们开发氢能、太阳能等新能源.