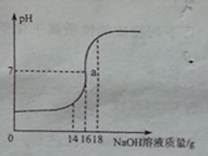
题目内容
水是常用的溶剂。如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
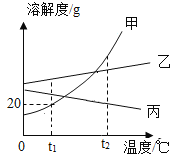
(1)t1℃时,将4.0 g甲物质放入10 g水中充分溶解得到________g溶液。
(2)若固体乙中混有少量固体甲,则提纯乙的方法是:溶解、_________、过滤。
(3)将t2℃时丙的饱和溶液降温到t1 ℃时,丙溶液溶质质量分数_________(填“变大”“变小”或“不变”)。
某化学学习小组的同学,为了比较铁、铜、锰三种金属活动性强弱,进行了下列实验探究:
(查阅资料)①铁的活动性比铜强;②锰在水溶液中反应通常显+2价。
(作出猜想)对三种金属活动性做出如下猜想:猜想Ⅰ.Fe>Cu>Mn; 猜想II. Mn>Fe>Cu;猜想III.________。
(进行实验)
实验操作 | 主要实验现象 | 结论及化学方程式 | |
1 | 将打磨好的银白色锰丝插入盛有硫酸铜溶液的试管中 | __________________ | 结论:Mn>Cu。 化学方程式为:__________________ |
2 | 将打磨好粗细相同的锰丝、铁丝,分别插入两份相同的稀盐酸中 | 锰丝表面产生气泡速率比铁丝________(填“快”或“慢”) | 结论:Mn>Fe。 写出其中一道反应的化学方程式:_____________ |
3 | 将打磨好粗细相同的锰丝、铁丝,分别在空气中点燃 | 锰丝在空气中剧烈燃烧,铁丝在空气中_____________。 | 结论:Mn>Fe |
(结论与交流)
(1)根据上述实验,猜想____________(填“Ⅰ”、“Ⅱ”或“Ⅲ”)正确。
(2)若要证明铁的活动性比铜强,可采用的实验方法是__________________。
归纳推理是学习化学的重要方法之一。下列有关事实和推理得到的结论合理的是
| 事实 | 结论 |
A | 二氧化锰对氯酸钾分解和过氧化氢分解均有催化作用 | 不同的反应有时可以使用同一种物质作催化剂 |
B | 白磷和红磷均是由磷元素组成的单质 | 白磷和红磷属于同一种物质 |
C | C与O2反应能放出大量的热 | C与O2不需要任何条件就可以发生反应 |
D | Al在常温下就能与O2发生发应,Fe在常温下几乎不与O2反应 | Al的抗腐蚀性能比Fe弱 |
A.A B.B C.C D.D
已知白磷的着火点为40℃,某化学兴趣小组为探究可燃物的燃烧条件,设计并进行了如下实验(实验过程中长颈漏斗下端始终在液面以下;注射器的摩擦力忽略不计):
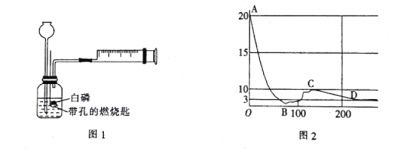
(1)实验前需要检验装置的气密性,写出检验该装置气密性的方法:______________。
(2)写出白磷燃烧的化学方程式:__________________________。
实验步骤 | 实验现象 |
①将白磷放在燃烧匙内,塞好胶塞 | |
②从长颈漏斗向瓶内迅速注入60℃的水至刚刚浸没白磷 | 白磷没燃烧 |
③连接好注射器,向瓶内推入空气,瓶内水面下降,停止推入空气 | 白磷燃烧,有白烟产生 |
④白磷熄灭后,瓶内水面上升,最后淹没白磷 | 白磷熄灭 |
(3)对比步骤②和③可知,可燃物燃烧条件之一是___________________,若把60℃的水换成20℃的水,重复实验步骤②和③,对比两次实验现象,还可以得出可燃物燃烧需要满足的条件是_______________。
(4)步骤④中瓶内液面上升,原因是____________________。
(实验拓展)用仪器测定白磷燃烧时集气瓶内氧气体积分数的变化,结果如图2所示[横坐标为反应时间(s),纵坐标为密闭容器中氧气的体积分数(%)]。
(5)通过分析数据,你对燃烧需要氧气有什么新的认识:___________________。
(6)分析图2中曲线变化趋势可知,在___________________(填字母)点时白磷全部熄灭。请解释曲线AB段、BC段、CD段的变化原因:
AB段:____________________________________________。
BC段:____________________________________________。
CD段:____________________________________________。
下列根据化学思维得出的结论正确的是
选项 | 方法 | 示例 |
A | 守恒法 | 2 克镁条在氧气燃烧所得固体质量为 2 克 |
B | 对比法 | 找出铁生锈的因素只需要做两个对比实验 |
C | 推理法 | 单质中只含一种元素,所以只含一种元素的物质就是单质 |
D | 归纳法 | 冰和干冰都是由分子构成的 |
A.A B.B C.C D.D