题目内容
(5分)有一包固体粉末A,可能是NaOH、Na2SO4、MgCl2、CuSO4中的一种或几种组成,为了分析固体粉末的成分,取少量该固体粉末进行实验,实验方案设计如下:
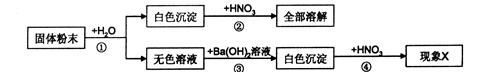
(1)A中一定含有 ,一定不含 。
(2)若X为“沉淀不溶解”或“沉淀部分溶解”,则A还含有 。若取消实验④,将③中的试剂换为 ,也可得出相同结论。
(3)写出②中化学反应方程式 。

(1)A中一定含有 ,一定不含 。
(2)若X为“沉淀不溶解”或“沉淀部分溶解”,则A还含有 。若取消实验④,将③中的试剂换为 ,也可得出相同结论。
(3)写出②中化学反应方程式 。
(1)MgCl2、NaOH;CuSO4 (第一空漏写不给分);(2) Na2SO4;BaCl2或Ba(NO3)2;
(3)Mg(OH)2+ 2HNO3= Mg(NO3)2+2H2O
(3)Mg(OH)2+ 2HNO3= Mg(NO3)2+2H2O
试题分析:(1)由实验①现象:“无色溶液”可知:A中一定不含硫酸铜;“白色沉淀”可知A中一定含NaOH和MgCl2有;(2)实验①反应后的溶液可能剩余氯化镁,加入氢氧化钡可以产生氢氧化镁沉淀,能溶于硝酸;若含硫酸钠,加入氢氧化钡,产生硫酸钡沉淀,不溶于硝酸,若X为“沉淀不溶解”或“沉淀部分溶解”则说明有硫酸钡沉淀,则A还含有硫酸钠;若X为“沉淀全部溶解”,则A中不含硫酸钠;可见实验④是验证硫酸钠是否存在的,若取消实验④,将③中的试剂换为可溶性的钡盐如BaCl2或Ba(NO3)2等,也可得到同样的结论;(3)氢氧化镁与硝酸发生中和反应,生成硝酸镁和水.

练习册系列答案
相关题目