题目内容
取13.8gR2CO3(R为未知金属元素)固体完全溶于水得到100g溶液,加入一定质量溶质质量分数为34.2%的Ba(OH)2溶液,恰好完全反应,过滤,得到BaCO3沉淀19.7g.向所得的滤液中滴入酚酞试液,溶液变红,逐滴加入20g一定溶质质量分数的稀盐酸,溶液刚好变成无色.试计算:(1)R的相对原子质量;
(2)所加Ba(OH)2溶液的质量;
(3)最后所得RCl溶液的溶质质量分数(计算结果保留一位小数).
【答案】分析:根据习题中恰好完全反应,利用R2CO3与Ba(OH)2溶液反应的化学方程式来计算R的相对原子质量及氢氧化钡溶液的质量为;再根据滤液中滴入酚酞试液,溶液变红,加盐酸溶液刚好变成无色所发生的反应来计算所得RCl溶液的溶质质量分数.
解答:解:(1)设R的相对原子质量为x,生成ROH的质量为y,氢氧化钡溶液的质量为z,
因R2CO3与Ba(OH)2溶液恰好完全反应,则
R2CO3+Ba(OH)2═BaCO3↓+2ROH
60+2x 171 197 2x+34
13.8g 34.2%z 19.7g y
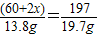
解得x=39,
即R的相对原子质量为39,
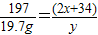
解得y=11.2g
答:R的相对原子质量为39.
(2)由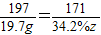
解得z=50g
答:Ba(OH)2溶液的质量为50g.
(3)设ROH与HCl反应生成RCl的质量为m
ROH+HCl═RCl+H2O
56 74.5
11.2g m
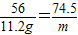
解得m=14.9g
则溶液中溶质的质量分数为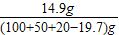 ×100%=9.9%
×100%=9.9%
答:最后所得RCl溶液的溶质质量分数为9.9%.
点评:本题考查学生利用化学方程式进行的有关计算,比较复杂,学生应正确利用恰好完全反应来判断能代入计算的物质的纯质量,还应注意利用总质量守恒计算最后所得溶液的质量,注意计算格式的规范性.
解答:解:(1)设R的相对原子质量为x,生成ROH的质量为y,氢氧化钡溶液的质量为z,
因R2CO3与Ba(OH)2溶液恰好完全反应,则
R2CO3+Ba(OH)2═BaCO3↓+2ROH
60+2x 171 197 2x+34
13.8g 34.2%z 19.7g y
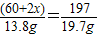
解得x=39,
即R的相对原子质量为39,
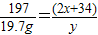
解得y=11.2g
答:R的相对原子质量为39.
(2)由
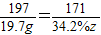
解得z=50g
答:Ba(OH)2溶液的质量为50g.
(3)设ROH与HCl反应生成RCl的质量为m
ROH+HCl═RCl+H2O
56 74.5
11.2g m
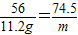
解得m=14.9g
则溶液中溶质的质量分数为
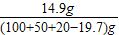 ×100%=9.9%
×100%=9.9%答:最后所得RCl溶液的溶质质量分数为9.9%.
点评:本题考查学生利用化学方程式进行的有关计算,比较复杂,学生应正确利用恰好完全反应来判断能代入计算的物质的纯质量,还应注意利用总质量守恒计算最后所得溶液的质量,注意计算格式的规范性.

练习册系列答案
相关题目