题目内容
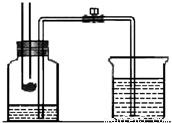
(2009?徐州模拟)某校化学学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出了如图
所示的实验装置.实验步骤如下:
①如图所示,连接仪器,检查装置的气密性.
②在集气瓶里装进适量a毫升的水,集气瓶剩余体积为V毫升,燃烧匙里放足量白磷,并在酒精灯上把玻璃棒下端加热,按图示装置把集气瓶中的空气密封起来,把长导管的另一端放入盛有足量水的烧杯中.(注:集气瓶内的长导管已伸到了瓶底.)
③把预先加热过的玻璃棒按下与白磷接触,观察到白磷立即着火燃烧,产生大量白烟,同时放出大量的热.
④待白磷燃烧熄灭后,稍加振荡,白烟消失.
⑤待集气瓶完全冷却至室温,量出集气瓶中水的体积.
根据以上信息,回答下列问题:
(1)白磷燃烧的化学方程式______ 2P2O5
【答案】分析:(1)白磷与氧气反应生成五氧化二磷;利用白磷和氧气反应放热、氧气的量约占空气体积的五分之一解决问题;
(2)围绕“降温以及吸收燃烧产物”这一因素进行分析;
(3)从使石蕊试液变红色的溶液显酸性的知识进行猜想.
解答:解:(1)①白磷立即着火燃烧,产生大量白烟,生成五氧化二磷,化学方程式为4P+5O2 2P2O5;
2P2O5;
②白磷燃烧放出大量的热,使集气瓶中压强增加,大于大气压强,液面下降,空气中的氧气被消耗,熄灭冷却后,集气瓶中的压强小于大气压强,液面上升,所以集气瓶中水面先下降后上升;
③由于氧气约占空气体积的五分之一,进入的水也是这一比例,则最终集气瓶中水的体积为:a+ v;
v;
(2)由于温度的改变会影响水的进入,所以需要使集气瓶温度尽快降低至室温,同时水也对吸收产物有一定作用.
“a体积的水”的作用,其一是为了加快⑤步骤中集气瓶的冷却速度;其二主要是吸收白磷燃烧生成的五氧化二磷; (3)小明的观点正确,白磷燃烧生成的五氧化二磷溶于水显酸性,滴加几滴紫色石蕊试液,会变红.
故答案为:
(1)4P+5O2 2P2O5,先下降后上升,a+
2P2O5,先下降后上升,a+ v;
v;
(2)吸收白磷燃烧生成的五氧化二磷
(3)小明,可能是白磷燃烧生成的五氧化二磷溶于水(或与水反应),导致溶液显酸性.
点评:空气中氧气含量的测定也是中考考查的一个热点,重点考查实验过程中看到的现象以及导致实验结果偏大或偏小的原因.
(2)围绕“降温以及吸收燃烧产物”这一因素进行分析;
(3)从使石蕊试液变红色的溶液显酸性的知识进行猜想.
解答:解:(1)①白磷立即着火燃烧,产生大量白烟,生成五氧化二磷,化学方程式为4P+5O2
 2P2O5;
2P2O5;②白磷燃烧放出大量的热,使集气瓶中压强增加,大于大气压强,液面下降,空气中的氧气被消耗,熄灭冷却后,集气瓶中的压强小于大气压强,液面上升,所以集气瓶中水面先下降后上升;
③由于氧气约占空气体积的五分之一,进入的水也是这一比例,则最终集气瓶中水的体积为:a+
 v;
v;(2)由于温度的改变会影响水的进入,所以需要使集气瓶温度尽快降低至室温,同时水也对吸收产物有一定作用.
“a体积的水”的作用,其一是为了加快⑤步骤中集气瓶的冷却速度;其二主要是吸收白磷燃烧生成的五氧化二磷; (3)小明的观点正确,白磷燃烧生成的五氧化二磷溶于水显酸性,滴加几滴紫色石蕊试液,会变红.
故答案为:
(1)4P+5O2
 2P2O5,先下降后上升,a+
2P2O5,先下降后上升,a+ v;
v;(2)吸收白磷燃烧生成的五氧化二磷
(3)小明,可能是白磷燃烧生成的五氧化二磷溶于水(或与水反应),导致溶液显酸性.
点评:空气中氧气含量的测定也是中考考查的一个热点,重点考查实验过程中看到的现象以及导致实验结果偏大或偏小的原因.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案
相关题目