题目内容
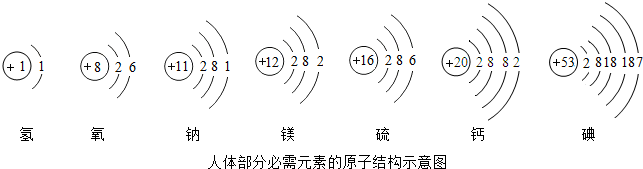
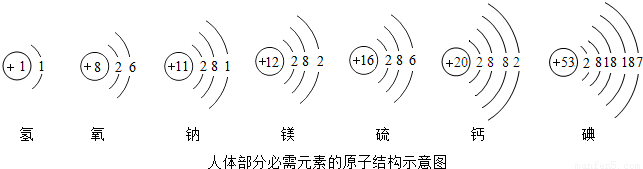
依图填空:

(1)硫离子的符号为 ,硫酸钠的化学式为 ;
(2)从原子结构上分析,图中钙、镁元素具有相似化学性质的主要原因是 ;
(3)生石灰(由图中某两种元素组成)常用作干燥剂,该干燥剂的吸水原理是 (用化学方程式表示);
(4)碘元素是人体必需的 (填“常量”或“微量”)元素,它处于元素周期表中的第 周期;由图中钙、碘、氧三种元素组成的碘酸钙[Ca(IO3)2]中,碘元素显 价。
【答案】
(1)S2﹣; Na2SO4;(2)它们原子核外的最外层电子数相同;(3)CaO+H2O=Ca(OH)2;
(4)微量; 五;+5
【解析】
试题分析:(1)依据硫的最外层电子数特点可判断硫离子带两个单位的负电荷,故硫离子的符号为S2﹣,由于硫酸根的化合价为﹣2价,钠元素的化合价为+1,所以硫酸钠的化学式为Na2SO4;
(2)依据最外层电子数相同时元素的化学性质相似分析解答。由于最外层电子数相同时元素的化学性质相似,故钙、镁元素具有相似化学性质;
(3)由于氧化钙能与水反应生成氢氧化钙,所以氧化钙能做干燥剂,其原理的方程式为CaO+H2O=Ca(OH)2;
(4)依据碘的核外电子数特点以及化学式中各元素的化合价代数和为零分析解答即可。碘是人体中必须的微量元素,碘的核外电子有5层,故它处于元素周期表中的第五层.在碘酸钙中钙显+2价,氧显﹣2价,依据化学式中各元素的化合价代数和为零,所以设碘的化合价为x,则有2+【x+(﹣2)×3】×2=0,解得x=+5;
考点:考查原子结构示意图与离子结构示意图;有关元素化合价的计算

练习册系列答案
相关题目