题目内容
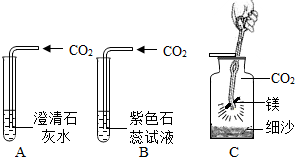 如图所示是有关二氧化碳的性质实验:(1)
如图所示是有关二氧化碳的性质实验:(1)| 实验序号 | 实验现象 | 实验结论:写反应式 |
| A | ||
| B |
(3)将镁条点燃后迅速伸入盛有CO2的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生炭和氧化镁,如C图.这个实验给你对过去某些知识的反思,从而有些新的结论发现:
考点:二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:(1)
A、二氧化碳与石灰水反应,瓶内压强变小,瓶子变瘪了;
B、二氧化碳与水反应生成了碳酸,碳酸能使紫色石蕊试液变成红色.
(2)根据碳酸不稳定,易分解解答.
(3)二氧化碳在特殊条件下能够支持燃烧;类比铁的燃烧实验可得细沙的作用.
A、二氧化碳与石灰水反应,瓶内压强变小,瓶子变瘪了;
B、二氧化碳与水反应生成了碳酸,碳酸能使紫色石蕊试液变成红色.
(2)根据碳酸不稳定,易分解解答.
(3)二氧化碳在特殊条件下能够支持燃烧;类比铁的燃烧实验可得细沙的作用.
解答:解:
(1)
A、由于二氧化碳与石灰水反应,瓶内压强变小,所以瓶子变瘪了.反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
B、二氧化碳与水反应生成了碳酸,碳酸能使紫色石蕊试液变成红色,反应的方程式是:CO2+H2O=H2CO3.
(2)给通过二氧化碳的B试管加热,可观察到的现象为:红色褪去,又恢复成紫色.产生这一现象的原因是碳酸不稳定,易分解.反应方程式是:H2CO3
CO2↑+H2O.
(3)通过该实验可知,CO2不支持燃烧存在片面性;二氧化碳在一定条件下也能支持某些物质燃烧,二氧化碳有时不能用来灭火等;燃烧时瓶底放沙一般都是防止炸裂瓶底,铁与镁的燃烧都是这个原因.
答案:
(1)
(2)红色褪去,又恢复成紫色 CO2+H2O=H2CO3
(3)CO2不支持燃烧存在片面性;二氧化碳在一定条件下也能支持某些物质燃烧 防止炸裂瓶底
(1)
A、由于二氧化碳与石灰水反应,瓶内压强变小,所以瓶子变瘪了.反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
B、二氧化碳与水反应生成了碳酸,碳酸能使紫色石蕊试液变成红色,反应的方程式是:CO2+H2O=H2CO3.
(2)给通过二氧化碳的B试管加热,可观察到的现象为:红色褪去,又恢复成紫色.产生这一现象的原因是碳酸不稳定,易分解.反应方程式是:H2CO3
| ||
(3)通过该实验可知,CO2不支持燃烧存在片面性;二氧化碳在一定条件下也能支持某些物质燃烧,二氧化碳有时不能用来灭火等;燃烧时瓶底放沙一般都是防止炸裂瓶底,铁与镁的燃烧都是这个原因.
答案:
(1)
| 实验序号 | 实验现象 | 实验结论:写反应式 |
| A | 瓶子变瘪了 | CO2+Ca(OH)2=CaCO3↓+H2O |
| B | 紫色石蕊试液变成红色 | CO2+H2O=H2CO3 |
(3)CO2不支持燃烧存在片面性;二氧化碳在一定条件下也能支持某些物质燃烧 防止炸裂瓶底
点评:本题主要考查二氧化碳、碳酸的化学性质,根据二氧化碳、碳酸的性质可以判断实验过程中能够观察到的现象.

练习册系列答案
相关题目
若铁原子的质子数为26,中子数为30,这种铁原子核外电子数为( )
| A、50 | B、56 | C、30 | D、26 |
下列变化中属于分解反应的是( )
| A、分离液态空气制氧气 |
| B、加热高锰酸钾制氧气 |
| C、蜡烛燃烧 |
| D、粗盐提纯 |
下列实验操作正确的是( )
| A、将实验室用剩的药品放回原瓶 |
| B、把鼻孔凑近瓶口闻药品的气味 |
| C、称量物质时,先加小砝码,再加大砝码 |
| D、玻璃仪器外壁有水,加热前应擦干 |