题目内容
【题目】将一定量铝粉和氧化铜混合加热,反应的化学方程式为3CuO+2Al![]() 3Cu+A12O3.反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中.下列叙述的现象中,能够说明氧化铜没有完全反应的是
3Cu+A12O3.反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中.下列叙述的现象中,能够说明氧化铜没有完全反应的是
①加入稀硫酸后,有气泡生成
②加入稀硫酸后,没有气泡生成
③加入稀硫酸后,溶液中有红色不溶物质
④插入溶液中的铁片表面有红色物质析出.
A.只有④ B.②③ C.③④ D.①③④
【答案】A
【解析】铝粉与氧化铜混合加热后会能生成铜和氧化铝.反应后的固体中一定有铜和氧化铝,也可能含有氧化铜或者是铝.往反应后的固体中加入足量的稀硫酸,铜不能与稀硫酸反应,故溶液中一定会有红色不溶物质.其中的氧化铝及可能剩余的铝能与稀硫酸反应生成硫酸铝,若有氧化铜剩余,能与稀硫酸反应生成硫酸铜溶液.充分反应后再插入铁片,可能剩余的稀硫酸会和铁片发生反应而放出气体,因此是否有气泡放出不能判断是否有氧化铜剩余.若铁片表面会析出红色的固体,则一定是与硫酸铜反应置换出来的铜,可能证明原固体中含有氧化铜.故选A.

【题目】珍珠粉由珍珠经加工制成的白色粉末,是重要的药品、化妆品原料.市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼无法辨别它们.但假珍珠使用过多会带来健康问题.

【提出问题1】珍珠粉的主要成分是什么?真假珍珠粉的差别在哪里?
【做出猜想】小明:含有碳酸钙;小华:含有蛋白质;小芳:含有碳酸钙和蛋白质
【实验一】为了确认珍珠粉的组成,他们进行了下列实验(表格如下):
操作 | 现象 | 结论 |
分别取真假珍珠粉个稍许置于两只试管中,加一定量的稀盐酸后迅速塞紧橡皮塞,将导管的另一端放入石灰水中,观察 | 试管a中均有气泡产生 试管b中实验现象 ; | 都含有碳酸盐 |
分别取真假珍珠粉稍许置于两只试管c、d中,滴加一定量的浓硝酸,静置后观察 | c试管能闻到烧焦羽毛的味道,d试管中未闻到烧焦羽毛的味道. | 假珍珠粉中不含 ; |
【结论】小芳的猜想成立.
【提出问题2】真假珍珠粉中碳酸钙的含量有差别吗?
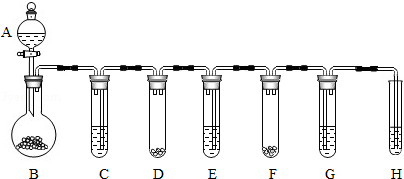
【实验2】各取5g真假珍珠粉各稍许,置于下列实验装置中(稀盐酸足量).测定生成气体体积数据如下:
样品种类 | 第一次 | 第二次 | 第三次 |
假珍珠粉样品(ml) | 110.50 | 110.28 | 110.05 |
真珍珠粉样品(ml) | 103.82 | 103.16 | 102.82 |
回答相关问题:
(1)实验前如何检查该装置的气密性 ;
(2)量气管点上端加一层植物油的目的是 ;
(3)由实验数据可知:真珍珠粉中碳酸钙的含量 假珍珠粉(填“>”、“<”、“=”).