题目内容
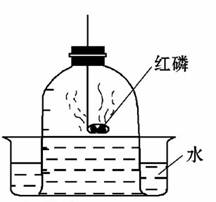
如图所示的装置也可用来测定空气中氧气的含量,对该实验的认识不正确的是( )
A.红磷的量不足会影响实验结论
B.装置不漏气是实验成功的重要因素之一
C.将红磷改为木炭也能得到正确的实验结论
D.钟罩内气体压强的减小会导致水面的上升
C

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
题目内容
如图所示的装置也可用来测定空气中氧气的含量,对该实验的认识不正确的是( )
A.红磷的量不足会影响实验结论
B.装置不漏气是实验成功的重要因素之一
C.将红磷改为木炭也能得到正确的实验结论
D.钟罩内气体压强的减小会导致水面的上升

C

 导学教程高中新课标系列答案
导学教程高中新课标系列答案