题目内容
 下列有两组实验,请根据实验中的问题回答.
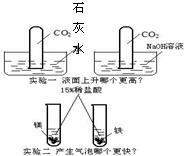
下列有两组实验,请根据实验中的问题回答.(1)写出实验一中左边装置中的实验现象:
试管内的液面上升
试管内的液面上升
;(2)写出实验二中“更快”的化学方程式:
Mg+2HCl=MgCl2+H2↑
Mg+2HCl=MgCl2+H2↑
.分析:(1)根据二氧化碳和水反应生成碳酸进行解答;
(2)根据镁的金属活泼性比铁的强,所以反应更快进行解答.
(2)根据镁的金属活泼性比铁的强,所以反应更快进行解答.
解答:解:(1)二氧化碳与水反应生成碳酸,试管内压强变小,所以试管内的液面上升;
(2)镁的金属活泼性比铁的强,所以反应更快,镁和盐酸生成氯化镁和氢气,化学方程式:Mg+2HCl=MgCl2+H2↑.
故答案为:(1)试管内的液面上升;(2)Mg+2HCl=MgCl2+H2↑.
(2)镁的金属活泼性比铁的强,所以反应更快,镁和盐酸生成氯化镁和氢气,化学方程式:Mg+2HCl=MgCl2+H2↑.
故答案为:(1)试管内的液面上升;(2)Mg+2HCl=MgCl2+H2↑.
点评:掌握二氧化碳以及金属的性质是解题的关键,属于基础知识的考查.

练习册系列答案
相关题目