��Ŀ����
Ԫ�������ɺ����ڱ����о���ѧ����Ҫ���ߣ��±���Ԫ�����ڱ��IJ�����Ϣ��
| 1 H �� |  | 2 He �� | |||||||
| 3 Li � | 4 Be �� | �� | 5 B �� | 6 C ̼ | 7 N �� | 8 O �� | 9 F �� | 10 Ne �� | |
| ll Na �� | 12 Mg þ | �� | 13 A1 �� | 14 Si �� | 15 P �� | 16 S �� | 17 C1 �� | 18 Ar � | |
| 19 K �� | 20 Ca �� | �� | | | | | | | |
��1���ؿ��к����ڶ��ķǽ���Ԫ�ص�ԭ���������� ����
��2��
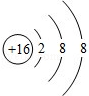 ��ʾ������ ����д���ӷ��ţ���
��ʾ������ ����д���ӷ��ţ�����3����9��20������Ԫ����ɵĻ��������� ����д��ѧʽ����
��4����ԭ�ӽṹ�Ƕȿ���ͬһ����Ԫ�ص�ԭ�Ӿ�����ͬ���� ������
��1��14����2��S2������3��CaF2�� ��4�����Ӳ�
���������������1���ؿ��к���ռ�ڶ��ķǽ���Ԫ��Ϊ�裬����Ԫ�����ڱ������ԭ������Ϊ14����2�������ṹʾ��ͼ��������Ϊ16������Ԫ�أ�����������Ϊ18��˵���õ�2�����ӳ�Ϊ�����ӣ��ʷ���ΪS2����3��9��Ԫ��ΪF��20��Ԫ��ΪCa����Ԫ���γɻ�����ʱF���ϼ�Ϊ��1�ۣ���Ԫ�صĻ��ϼ�Ϊ+2�ۣ���ѧʽΪ��CaF2��4����ÿһ���ڵ�ԭ�ӽṹʾ��ͼ�������ѿ�����ͬһ����Ԫ�ص�ԭ�Ӿ�����ͬ�ĵ��Ӳ�����
���㣺Ԫ�����ڱ����ص㼰��Ӧ�ã�ԭ�ӽṹʾ��ͼ�����ӽṹʾ��ͼ����ѧʽ����д�����壮

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
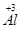
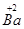
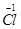 SO42-
SO42-