题目内容
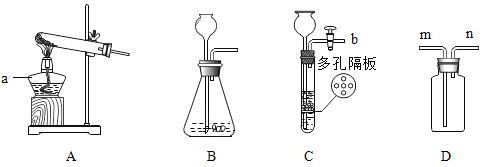
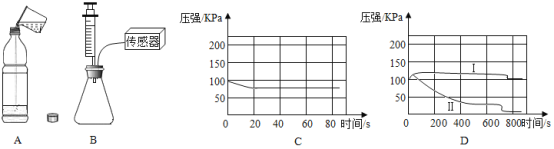
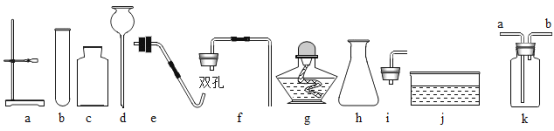
【题目】实验室有高锰酸钾、稀盐酸、澄清的石灰水、氯酸钾、过氧化氢、二氧化锰、大理石,下列仪器及相关用品:
(1)用上述一种药品在实验室制取氧气的化学方程式为_____;导管口开始有气泡时,不宜立即收集。原因是_____当气泡连续且比较均匀放出时,再把导管口伸入_____,开始收集。
(2)实验室制取二氧化碳,并可以随时添加稀盐酸,选择的仪器是_____(填字母,选择一种合理情况即可),若选用k装置采用排空气法收集二氧化碳,气体应从_____(填“a”或“b”)导管口通入。若选用k装置验证二氧化碳,其中的药品名称是_____。
(3)实验室制取二氧化碳气体的过程中,锥形瓶内气体能够导出的原因是,瓶内发生化学反应,使_____压强变_____,在压强差的作用下,气体导出。
【答案】2KMnO4![]() K2MnO4+ MnO2+O2↑(合理即可) 刚开始排出的气体是空气不能收集 盛满水的集气瓶中 cdfh(或abcdf) a 澄清石灰水 气体增多 大
K2MnO4+ MnO2+O2↑(合理即可) 刚开始排出的气体是空气不能收集 盛满水的集气瓶中 cdfh(或abcdf) a 澄清石灰水 气体增多 大
【解析】
(1)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为2KMnO4![]() K2MnO4+ MnO2+O2↑;当导管口有连续均匀气泡时,再把导管口伸入盛满水的集气瓶中,因为刚开始排出的气体是空气不能收集;停止加热时,需先把导管移出水面,然后再熄灭酒精灯,防止因停止加热后试管内不再产生气体且温度下降,压强减小,小于外界大气压,在压强差的作用下,水槽里的水倒流炸裂试管;故填:2KMnO4
K2MnO4+ MnO2+O2↑;当导管口有连续均匀气泡时,再把导管口伸入盛满水的集气瓶中,因为刚开始排出的气体是空气不能收集;停止加热时,需先把导管移出水面,然后再熄灭酒精灯,防止因停止加热后试管内不再产生气体且温度下降,压强减小,小于外界大气压,在压强差的作用下,水槽里的水倒流炸裂试管;故填:2KMnO4![]() K2MnO4+ MnO2+O2↑;刚开始排出的气体是空气不能收集;盛满水的集气瓶中
K2MnO4+ MnO2+O2↑;刚开始排出的气体是空气不能收集;盛满水的集气瓶中
(2)实验室制取CO2 ,是在常温下用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。若用排气法收集气体,并在实验过程中可以随时添加液体,则可选择的仪器或装置组合c、 d.、f、h(或abcdf) ;欲使用装置k用排空气法收集二氧化碳,因为二氧化碳密度比空气大,则气体应从长管a端通入,若检验二氧化碳,要用澄清石灰水,二氧化碳可以和氢氧化钙反应生成碳酸钙沉淀和水,使澄清石灰水变浑浊,故填:
c、 d.、f、h(或abcdf);a;澄清石灰水;
(3)实验室制取二氧化碳气体的过程中,锥形瓶内气体能够导出的原因是,瓶内发生化学反应,使气体增多压强变大,在压强差的作用下,气体导出,故填:气体增多;大:

 教材全解字词句篇系列答案
教材全解字词句篇系列答案