题目内容
【题目】如图为六种原子的结构示意图.
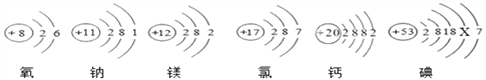
请回答下列问题:
(1)图中六种元素之间的最本质区别是__不同。
(2)氧化钠由钠离子和氧离子构成,氧化钠的化学式为__;
(3)从原子结构上分析,图中具有相似的化学性质的元素是__和__(填元素符号)
(4)在上述碘的原子结构示意图中,X=__.
【答案】 质子数 Na2O Cl I 18
【解析】在原子结构示意图中,小圆圈表示原子核,圆圈内的数字表示质子数,质子数决定原子的类别,弧线表示电子层,最外层电子数决定原子的化学性质,质子数决定原子的类别。原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构;具有稳定结构的原子化学性质相似;非稳定结构的原子,最外层电子数一样的化学性质相似。(1)元素之间的最本质区别是质子数不同;(2)氧化钠由钠离子和氧离子构成,氧显﹣2价,钠为+1价,所以氧化钠的化学式为:Na2O;(3)从原子结构上分析,氯与碘原子的最外层的电子数相同,元素具有相似的化学性质,元素符号分别为:Cl、I;(4)由于在原子中,核内质子数=核外电子数,在上述碘的原子结构示意图中,x=53﹣2﹣8﹣18﹣7=18。

【题目】通过联想提出问题是探究的源泉,某合作学习小组开展了如下探究,请你协助他们完成:

【提出问题】温度越高,分子运动越快;温度越高,化学反应也越快吗?
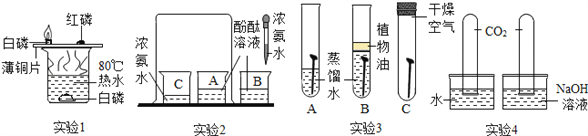
【实验探究】为了探究温度对H2O2分解反应速率的影响,某实验小组使用如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分数据如表所示:
实验1 | 实验2 | |
MnO2的质量/g | 0.5 | 0.5 |
5%的H2O2的体积 /mL | 40 | X |
恒温水浴加热/℃ | 40 | 80 |
收集一试管氧气所需要时间/ 秒 | 36 | 23 |
(1)实验2中X=____;
(2)在两次实验中,记录不同温度下收集同体积的氧气所需要时间的实验设计目的是______;还可以_______________________ 达到相同的目的,
【实验结论】通过两次实验的实验记录,你可以得出的实验结论是:_________________ ;
【实验拓展】请根据所学再举出一例与温度有关的实验结论:温度越高,_________。
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )

温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A. 乙为NH4Cl
B. t3应介于40℃﹣50℃
C. 55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙
D. 等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等