题目内容
 右图为甲、乙、丙三种物质的溶解度曲线,据图回答:
右图为甲、乙、丙三种物质的溶解度曲线,据图回答:(1)要提纯含有少量乙的甲物质,通常采用的方法是
(2)t1℃时将等质量三种物质的饱和溶液,升温至t3℃时,其溶液的质量关系为
(3)将20克甲物质完全溶解于100克水中,不能形成饱和溶液的温度范围是
分析:(1)根据提纯的物质的曲线变化情况考虑;(2)根据t1℃时将等质量三种物质的饱和溶液,升温至t3℃时,晶体的析出情况考虑;(3)根据将20克甲物质完全溶解于100克水中形成饱和溶液的温度范围来考虑.
解答:解:(1)由题意提纯含有少量乙的甲物质,可知提纯的是甲物质,由于甲的溶解度随温度的变化比较大,所以用冷却热饱和溶液的方法使溶质结晶析出;
(2)t1℃时将等质量三种物质的饱和溶液,升温至t3℃时,甲和乙都变为不饱和溶液,溶液质量不变,丙的溶解度减小会析出晶体,溶质减小,溶液质量也就减少了,所以甲=乙>丙;
(3)由于20克甲物质完全溶解于100克水中恰好达到饱和时,说明该温度时它的溶解度是20g,通过曲线图可知t2℃甲的溶解度为20g,小于这一温度,溶解度也小于20g,都属于饱和状态,大于这一温度时,溶解度大于20g,这时就属于不饱和状态了.
故答案为:(1)冷却热饱和溶液(或降温结晶);(2)甲=乙>丙;(3)>t2.
(2)t1℃时将等质量三种物质的饱和溶液,升温至t3℃时,甲和乙都变为不饱和溶液,溶液质量不变,丙的溶解度减小会析出晶体,溶质减小,溶液质量也就减少了,所以甲=乙>丙;
(3)由于20克甲物质完全溶解于100克水中恰好达到饱和时,说明该温度时它的溶解度是20g,通过曲线图可知t2℃甲的溶解度为20g,小于这一温度,溶解度也小于20g,都属于饱和状态,大于这一温度时,溶解度大于20g,这时就属于不饱和状态了.
故答案为:(1)冷却热饱和溶液(或降温结晶);(2)甲=乙>丙;(3)>t2.
点评:在提纯物质时关键看所提纯的物质溶解度的变化情况,溶解度随着温度变化大的用冷却热饱和溶液的方法,溶解度随着温度变化不大的用蒸发溶剂的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
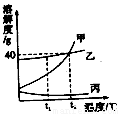
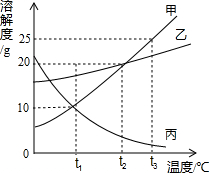 右图为甲、乙、丙三种物质的溶解度曲线,据图回答:
右图为甲、乙、丙三种物质的溶解度曲线,据图回答: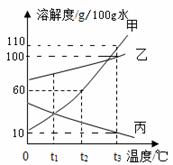 右图为甲、乙、丙三种不含结晶水的固体物质溶解度曲线,据图回答:
右图为甲、乙、丙三种不含结晶水的固体物质溶解度曲线,据图回答: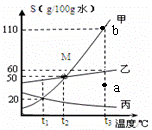 ① t1℃时,甲、乙、丙三种物质的溶解度由大到小的
① t1℃时,甲、乙、丙三种物质的溶解度由大到小的