题目内容
近几年,为了使汽油燃烧的更加充分而且减少燃烧过程产生的有害物质,人们在汽油中点燃掺入一定量的乙醇并称之为乙醇汽油.乙醇燃烧的化学方程式为:C2H5OH+xO2
2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为( )
| 高温 |
| A.3mol | B.6mol | C.7mol | D.6.5mol |
根据氧元素原子个数守恒,可知氧气的配平系数为3,
根据方程式中各物质的化学计量数之比即为各物质的物质的量之比,
可得出每消耗2mol乙醇需要氧气为2×3mol=6mol
故选B
根据方程式中各物质的化学计量数之比即为各物质的物质的量之比,
可得出每消耗2mol乙醇需要氧气为2×3mol=6mol
故选B

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
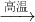 2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为
2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为 2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为( )
2CO2+3H2O,则每消耗2mol乙醇,需要氧气的物质的量为( )