题目内容
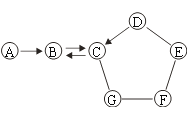
【题目】右图中:A、B、C、D、E、F、G是初中化学常见的物质,其中A为单质,B为氧化物,C是大理石的主要成分,C和F属于不同类别的物质,实验室用C和G制B,D和E是配制农药波尔多液的两种原料,其中D可用于改良酸性土壤,E可用于游泳池消毒,“—”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质。请回答:
(1)D和E发生反应的基本反应类型为 ;
(2)完成下列化学方程式:
① A→B的化学方程式:_______________________
② C→B的化学方程式:______________________
(3)物质F可以是 或 (具体写两种不同类别的物质)
(4)A、B、C、D、E、F、G七种物质中属于盐的物质有 种。
【答案】(1)复分解反应
(2)①C+O2![]() CO2(合理即可)②CaCO3
CO2(合理即可)②CaCO3![]() CaO + CO2↑
CaO + CO2↑
(3)NaOH,Fe(4)2
【解析】
试题分析:D和E是配制农药波尔多液的两种原料,D可用于改良酸性土壤,说明D是氢氧化钙,E是硫酸铜溶液,C是大理石的主要成分,说明C是碳酸钙,实验室用C和G制B,且B是一种氧化物,说明B是二氧化碳,而G是盐酸,A是一种单质,能够反应得到二氧化碳,说明A是碳,E是硫酸铜而G是盐酸,都能够和F反应,说明F是一种金属或者一种碱,所以可能是NaOH,Fe; 所以A、B、C、D、E、F、G七种物质中属于盐的物质有2中。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3: ①
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | ② | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量 ③ | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入 ④ | ⑤ |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 ⑥ .
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为 ⑦ ⑧
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 ⑧ 碱性氧化物(填“是”或“不是”).